782
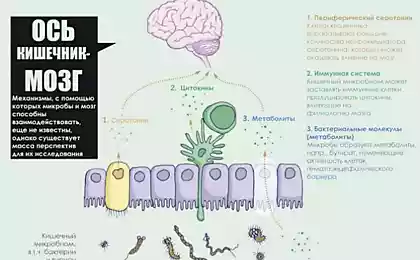
Почуття кишечника: про зв'язок мікрофлори кишечника і функцій мозку
Замітка редактора в оригінальній: осі Гута-браїна є явним зв'язком і одним з нових горизонтів комплексу нейронауки. Мікробіота кишечника, часто називають «другим геном» і «другим мозком», може впливати на наш настрій через механізми, які вчені просто починають розуміти. І на відміну від генів ми успадкуємо, мікробіота може бути змінена і навіть вирощена. Як дослідження зрушуються з нелюдського мишей, ми отримуємо більше розуміння зв’язків мікробіота до наших мозків, а важливі зв’язки до психічного (або психічного) здоров’я стають очевидними.
Відео з www.npr.org
Примітка: в оригінальній статті можна знайти примітки (живі посилання на дослідження).
Я вчений, і часто навіть у розмовах з сусідами засмагає щось нові досягнення в нейронауці. І в останні кілька років я помітив, що більше і більше людей цікавляться мікробіом - мікроорганізмами, які збільшують наші тіла, наші органи. За останні 10 років я працюю в області, де ми розробляємо нові припущення щодо того, як мікробіота кишечника впливає на роботу мозку. Тепер це вже написано в пресі, включаючи Нью-Йоркські часи (переклад цього матеріалу доступний на сайті ECOWAYS, див.). Тег "мікрофлора" і в Національній географічній. У 2012 році редактори журналу «Наука» вважають, що це важливо для того, щоб присвятити всім питанням темі.
Чому ми знаходимо цю тему так захоплюючим? Для початківців рівень свідомості в харчуванні підвищується: ми докладаємо ближче, щоб розпізнати здоров’я раціону та раціони. Крім того, подивіться на номери! Мозок складається з мільярдів нейронів, і є трильйони «добрих» бактерій в кишечнику, але ми говоримо про них значно рідше. Зрозуміло, це ці бактерії, які природним чином вводять нас, які завжди присутні в нашому «симбіонти» (дружні бактерії, життєві функції яких отримують хост) можуть стати інструментом або інструментом, який впливає на розвиток наших мозку, формування нашої поведінки і стресових відповідей, що впливають на те, як наш організм отримує лікування (наприклад, ліки для депресії або тривожності).
З огляду на такі серйозні наслідки на психічне здоров’я, в науковому середовищі тема взаємовпливу цього умовно вічного зв’язку привертає більше уваги. Я завжди вражаюсь на вроджених методах, колеги приступають до дослідження, особливо для вивчення того, як мікробіота може вплинути на мозок і імунітет на ранні роки життя. І всього минулого тижня вчені UCLA виявили, що регулярне споживання йогурту з живими пробіотиками (тобто, що містять «добрі» бактерії), схоже, впливають на роботу мозку жінок.
Причини і наслідки
Вчені визнали зв'язок між мозку і кишечником понад сто років тому: вже на початку XIX століття, а потім знову, на початку XX, доведено, що емоційний стан людини може вплинути на роботу кишечника (1-3) Одним з кращих прикладів цього є робота Вільяма Баумонта, військового хірурга, який став відомий як «шкіра гастрофізіології». У 1830-ті рр. у нього було можливість спостерігати секретацію шлунково-кишкових соків через фістулу (постійну через отвір в шлунку пацієнта). І в першій декаді ХХ ст. вони дивилися на вплив стресу на організм і здоров'я людини і знайшли зв'язки між якістю реагування людини на стрес і як працює кишечник. Це класичне розуміння вертикальної системи управління (тобто, що мозок впливає на функціонування інших органів, в тому числі кишечника) посилюється тим, що команди з мозку до тіла, включаючи команди до кишечника, передаються через нервові зв'язки вегетативної нервової системи і через гуморальні системи в кровоплині. Обидва ці канали зв'язку активуються в період стресу і впливають на травну систему. Зрозуміло, і нова в цій історії, ми зараз почали розглянути неперевершені зв'язки, «знизу» – тобто ми виявили, що кишечник, а точніше, мікрофлора кишечника, може вплинути на функціонування мозку. Останнім часом вчені довели, що наявність мікрофлори кишечника на ранньому етапі розвитку впливає на топологію нейронів (комплект властивостей цілих частин мозку) пов'язаних з тривожністю і депресивними станами. Мікрофлора кишечника пов'язана з специфічними поведінками, стресами та захворюваннями стресу. Зміна мікрофлори кишечника може впливати на ризик розвитку захворювань, а мікрофлора управління може стати новим методом втручання в ситуації, які вже досягнути клінічного етапу (у сфері торкнених і тривожних порушень).
Внутрішнє фарбування
Нормальний симпіонат (дружній) мікрофлора розсмоктує кишечник ссавців та інших внутрішніх зон тіла коротко після пологів і псистів в організмі протягом усього життя. Людина в товстому кишечнику (в нижніх частинах) містить бактерії від 10 до 14-го до 10 до 15-го ступеня, тобто в кишечнику 10 або навіть 100 разів більше бактерій, ніж клітини в нашому організмі (4).
Співіснування мікрофлори і його носія, для найбільшої частини, взаємовигідного. Зокрема, наявність симпіонів є важливим для функціонування нашої імунної системи, обробки поживних речовин та інших аспектів здорової фізіології. (5, 6) Використання найсучасніших інструментів для вивчення генетики та тканин тіла на молекулярному рівні вчені змогли продемонструвати, що є кілька типів бактерій в кишечнику, і що популяції симбіонта дуже різноманітні: до тисячі різних видів можна виділити (7). Крім того, формування індивідуальної мікрофлори постійно впливає на фактори, такі як гендер, генетика, вік, дієта (8, 9). У здорових людей бактеріологічна різноманітність набагато більше, але в той же час вивчення мікрофлори таких людей в різний час (з інтервалом декількох місяців можна побачити, що композиція навряд чи змінюється). (4, 10, 12) Але в стресових ситуаціях або у відповідь на фізіологічні або харчові зміни, сама мікрофлора може змінитися, створюючи дисбаланс взаємодії мікрофлори і її носія. І такі зміни можуть вплинути на стан здоров’я людини.
Я бачу світло!
Неперервна мікрофлора дуже важлива для здорового розвитку мозку. Наприклад, це може вплинути на розвиток частин мозку, в яких утворюється стресова відповідь – області, які контролюють стресоіндуковані умови, такі як тривожність або депресії. У спробі зрозуміти ці взаємини, вчені утворюють мікрофлору в мишей: спеціальні, «стерильні» мишей з абсолютно відсутніми мікрофлори вирощуються в ізоляторах, а потім на них виготовляються різні бактеріальні вимірювання.
Затримка в ізоляторі виключає будь-який контакт з зовнішнім повітрям, будь-які домішки або симпіонати бактерії ззовні. Потім проводиться стандартні експерименти для вивчення змін поведінки: рівень активності, curiosity і схильність до уникнення контакту вимірюється. Мишей має природну схильність до вивчення їх діапазону, але вони завжди намагаються уникнути відкритих і яскраво освялених місць. Їхня поведінка тестується в спеціальному «мазе», призначеному таким чином, що мишей має можливості показати свої наукові інтереси. Коли звичайна (контролю) миша надходить в цю масу, вона намагається вивчити як «подушки», які простягаються в будь-якому напрямку з зони, в якій спочатку «засаджується» в центрі. У той же час миша прагне витрачати більше часу на вивчення закритого, затемненого рукава. Коли стерильна миша розміщується в маслі, вона прагне витрачати більше часу на освітлений рукав. І це призводить до припущення, що без мікрофлори менша тривожність, оскільки стерильні мишей витрачають більше часу в «небезпечні» зоні мажори. 13, 14.
Для іншого поведінкового тесту, коробка використовується в якій одна частина затемнена і друга частина відкрита до світла. Контрольна миша досліджує як ділянки, але приділяє більше уваги темряві. Стерильний мишей досліджує світлу площу довше, знову демонструючи, що мишей без мікробіоти не схильні до тривоги, оскільки світлозона для мишей в експерименті вважається стресовим, але стерильні мишей не турбуються цим.
За допомогою стерильної мишеї дослідники змогли дізнатися, чи були конкретні етапи в житті миша, коли особливо важлива взаємодія мозку та флора кишечника. Стерильні мишей розміщені в нормальних умовах для мишей на різних «вагах» (на різних стадіях їх розвитку) і виявили, що їх кишечники були загиблими типовими популяціями бактерій. Так само було відображено в нормалізації підрозробної імунної системи, характерної для стерильних мишей. Коли стерильні дорослі колонізували з нормальними бактеріями, вони продовжували показувати знижені рівні тривожності, припускаючи, що відсутність мікробіоти на ранньому розвитку має постійний вплив на те, як мозок регулює тривожність і поведінки, пов'язані з розвідувальним імпульсом. (14, 16)
На відміну від того, коли мікробіота була колонізована в стерильних мишей рано в їхньому житті (молодий або новозрілий) і потім випробувана на зрілість, мишей, як правило, показали нормальні рівні стресу і тривожності в стресових ситуаціях (13, 15) і це говорить про те, що мікробіота впливає на те, як мозок утворюється ранньо в житті. (17)
На додаток до досліджень в мишей науковці застосовують антибіотики для впливу мікрофлори. Показана наявність антибіотиків у питній воді для зменшення бактеріальних популяцій у мишей та зменшення різноманіття в межах цього населення. (18) Тести показали, що як стерильний мишей, так і ті, які лікують антибіотиками на тиждень, показали підвищену життєздатність (активацію наукової поведінки) і зниження тривожності. Це спостереження пов'язане з змінами мікрофлори. (19) Два тижні після закінчення тижня на антибіотики, як мікробна якість і поведінка були відновлені до нормальних рівнів, і це говорить про те, що тимчасові зміни мікробіоти можуть вплинути на поведінку. (19)
У правому варіанті.
Встановивши взаємозв'язок мікрофлори кишечника, мозку і поведінки, цікаво подумати про те, як, власне, мікрофлора «комунікації» з мозку. Звичайно, класична теорія полягає в тому, що нервові з'єднання передають сигнали до мозку від нервових закінчень (фізична нервова система), а зокрема так званого нерва, який передає сигнали до мозку з кишечника. Відсутність, що бактерії в кишечнику можуть діяти шляхом відправки сигналів, використовуючи цей зв'язок ілюстровано наступним експериментом: мишей були «заплановані» з хвороботворними бактеріями, такими як цитентій Citrobacter і Campylobacter jejuni, і це активовано «канал зв'язку», пов'язаний з ваговим нервом і відповідними зонами в мозку.(20, 21)
Цей нейронний зв'язок був знайдений для активації навіть при відсутності периферичної імунної реакції, що передбачає прямий зв'язок між бактеріями кишечника і нервовою системою. Недавнє дослідження встановлено, що годування здорових мишей з пробіотиками — тобто «добрих бактерій» — зниження тривожності та депресивної поведінки порівняно з контрольною групою (22), а ще одне дослідження виявило, що підживлення пробіотиків активовано нейронів у гіпоталаму, області мозку, що відіграє важливу роль у стресовій відповіді. (23)
У цьому дослідженні активація нейронів у гіпоталамусу була більш інтенсивною, коли мишей дали патогенні бактерії, і це призвело до більш активної периферичної імунної реакції. Це говорить про те, що обидва периферичні нервові закінчення і імунні молекули в крові, які передають сигнали можуть сприяти зв'язуванню кишечника і мозку. (23) Гіпоталамус є автономним центром контролю нервової системи, і є сильні докази, що психологічні, фізіологічні та патологічні проблеми можуть активувати гіпоталамус і викликати «спадкову відповідь». Сприяє активації цієї критичної області в мозку.
Ця робота визначає, як відбувається з'єднання кишечника і мозку на рівні невралу, але є ще один важливий канал комунікації: імунітет. Його можна назвати двома компонентами: сама і адаптивна імунна система - набутий імунітет. У стерильних мишей не розвинена адаптивна імунітет. Оскільки мікрофлора кишечника відіграє ключову роль у розвитку імунітету, можна вважати, що запальні процеси стерильних мишей завжди спокійні. Коли ми розглянемо посилання між запаленням і тривожною поведінкою, ми можемо спостерігати, що низька тривожність виявлена, де запальні процеси сильно виражені, але сильні запалення призводять до підвищеної тривожності. (17)
Наприклад, зараження мишей з паразитом тричуріса призводить до запалення в кишечнику і підвищених рівнів тривожності.(24) Крім цього, хімічно спровоковані запалення (коліт) також призводить до підвищеної тривожності. 24 мар Те ж саме дослідження дають докази, що мікробіота виступає модулятором цієї тривожності в пов'язаних з імунітетом поведінки: звіти говорять, що «лікування» з пробіотичної культури Bifidobacterium longum знизив цю тривожність. (24.25) Ці спостереження свідчать про те, що пробіотики можуть довести перспективу при лікуванні запальних процесів або пов'язаних симптомів «аксити». й
Симбіонт бактерії відіграють важливу роль у забезпеченні здоров'я кишечника, а в стресових ситуаціях або при захворюваннях підвищена проникність кишечника може сприяти підвищенню запалення. (26), підвищена проникність стін кишечника (зазначено як «синдром голоду») може призвести до передачі бактерій за межами кишкового тракту до «зовнішного» середовища.
Це додатковий шлях, що мікробіота (мікрофлора) і патогенні бактерії можуть використовуватися для спілкування з мозку, де імунна система стає каналом спілкування, або це відбувається шляхом активації нейронів місцевої вегетативної нервової системи. Він, в свою чергу, є частиною вегетативної (генетичної вегетативної) нервової системи, що базується в кишечнику і відповідає за перистальтику і нормальне здійснення інших функцій кишечника. (28) Це велика мережа нейронів, які виступають в якості першого посилання в контакті між мікрофлорою кишечника і мозку, вони є важливою складовою в зв'язці мозку.
фактор стресу
Одним з найбільш поширених ознак депресії є розлад в системі, відповідальний за стресову відповідь, на основі «віси» надниркових залоз.(29) Як зазначено вище, у відповідь на фізіологічний, психологічний або патологічний стимул, нейрони в гіпоталаму активуються і надсилають сигнал до гіпофіза, який викликає введення адренакортикотропного гормону в кров, який в свою чергу активізує надниркових залоз, щоб вони терміново випустили стресовий гормон кортизол. Ця «спадкова відповідь» є частиною нормального процесу, але при депресії, вона часто викликається занадто швидко або, іноді реакція занадто луглива. (29) Одним з перших досліджень, які шукають відносини між стресом і мікробіота, показали, що стерильний мишей мав надмірно інтенсивну відповідь на стрес.(23) І ще, більш недавнє дослідження показали, що вплив на стрес у щурів «у молоді» викликає порушення в складі мікрофлори і призводить до більш інтенсивних стресових реакцій у дорослому віці. (30) Важливо, що це дослідження виявило, що дає щурам пробіотики (Лактобацил) нормалізованих рівнів гормону стресу. 30 Стрес рано в житті призводить до більш депресивної поведінки в зрілих щурів. Ще одним аналогічним дослідженням стало те, що при стресових щурів були дані пробіотики (біфіодні бактерії), ознаки депресії знизилися в дорослому віці. (31)
Разом з тим, ці дослідження свідчать про те, що зв’язок між мікробіальним дисбалансом (дисбіозом), зміни поведінки, пов’язані з стресом та реагуванням на стрес. Також пропонується, що використання пробіотиків може бути ефективним при лікуванні стресових симптомів.
На даний момент існує кілька досліджень, які пов'язують стрес і мікрофлора у людини. Не існує даних про прямі зв'язки між складом мікрофлори та депресивними розладами або тривожними станами. Найперспективніші клінічні дослідження свідчать про те, що застосування пробіотиків у людини може мати антидепресантний і седативний ефект. У яких здорових людей дали пробіотики протягом 30 днів. Предмети були запропоновані відповісти на ряд питань, щоб визначити наслідки: увага зверталася до стресостійкості, тривожності, симптомів депресії, потенціалу протистояти стресу. Результати показали, що ті, хто отримав пробіотиків, показали меншу стресову активність, ніж контрольна група.(32) У іншому дослідженні дослідники змогли продемонструвати, що здорові люди з низькими настроями на старті експерименту показали поліпшення настрою після прийняття пробіотиків протягом трьох тижнів.(33) Нарешті, в клінічному дослідженні людей з синдромом хронічної втоми, прийом пробіотиків протягом 2,5 місяців знижується тривожно-пов'язані симптоми.(34) Ці дослідження показують, що сучасні клінічні дослідження підтверджують важливу роль мікрофлори при формуванні тривожності і депресії. Вони також демонструють потенціал для лікування пробіотиків.
Проспекти
Не сумнівайтесь, що протягом останнього десятиліття дослідження було створено чітке посилання між мікробіотапом кишечника та функцією мозку у мишей. Ми зрозуміли, що:
1) мікрофлора кишечника (мікробіота) – величезне населення, важливе для здорового обміну речовин і функції мозку
2) зв'язок кишечника і мозку, в тому числі через нервові з'єднання
(3) Неперевершений мікробіота дуже важливий у ранньому віці і може впливати на які стресові відповіді виробляються в мозку.
4) пробіотиків (гуман і тваринні дослідження показали, що пробіотики або «добрих бактерій», позитивно впливають на настрій. І в той час як це дуже перспективні відкриття, не потрібно худнути і думати, що ми вже знайшли рішення для клінічних ситуацій (ведучих і розладів настрою). Звичайно, мікробіота є важливим модулятором здоров'я і слід враховувати складну, багатогранну систему зв'язку, яка необхідна для створення здорового балансу для розвитку і здорового функціонування мозку. Зараз дослідження в цій області ведеться по всьому світу – вчені прагнуть зрозуміти якомога більше. Слідкуйте за новинами! Видання
Автор Джейн Фостер (Джан Фостер)
Оригінальна стаття: dana.org/news/cerebrum/detail.aspx?id=44080
За посиланням на оригінал англійською мовою також можна побачити в усній формі всі посилання на наукові дослідження, позначені в нашому перекладі з номерами в дужках.
P.S. І пам'ятайте, що просто змініть наше споживання – разом ми змінюємо світ!
Джерело: Ecoways.ru/en/rss/articles/o_svazi_mikroflori_i_funktsij_golovnogo_mozga.html