525
Метаболічна пам'ять: помста подається холодним
Гляка веде не тільки структурні, але й функціональні зміни в багатьох елементах тіла. Більш того, ці зміни можуть бути довгостроковими, з декількох місяців до декількох років (6 років і більше). Зателефонована метаболічна пам'ять, сьогодні я збираюся говорити про те, як глікація може змінити нормальний метаболізм клітин і чому зміни способу життя може не завжди працювати відразу.
Гляка довголічених білків і ДНК - це процес, який невидимий спочатку, але дуже важко ремонтувати пізніше. Так, глікозинні кінцеві продукти дуже вироковані, а помста - це блюдо, подається холодним.

Що таке метаболічна пам'ять?
У дослідженні цукрового діабету з'явився термін «метаболічна пам'ять». Справа в тому, що, незважаючи на досягнення в лікуванні захворювання - розвиток нових цукрово-жовтих агентів, досягнення успішного контролю глікемії і визначення маркерів глікемії, більшість пацієнтів розвиваються серйозні ураження органів призначення, що призводять до серйозних ускладнень.
Метаболічна пам'ять (відоме як гіперглікемічна або судинна пам'ять) є ефектом, що призводить до розвитку довгострокових ефектів тривалого періоду погано компенсованого рівня глюкози крові. Іншими словами, довший цукровий діабет залишається некомпенсованим, чим довше цей шкідливий ефект зберігається, навіть після кращого контролю захворювання.
Спочатку ранні епізоди гіперглікемії негативно впливають на рівень ретинальних клітин, нирок, а також функціонування нервових волокон. «Метаболічна пам'ять» – це ситуація, де збільшення глікемії – навіть перед постановкою діагнозу захворювання – вже патологічно впливає на різні системи організму.Особливо на нервових волокнах. Більш того, якщо глікозний контроль був недостатнім протягом тривалого часу, ефект пошкодження може зберігатися в майбутньому, навіть після оптимізації рівня глюкози.
Зокрема, у великому дослідженні АДВАНС було виявлено, що суворий контроль глікемії у цукровому діабеті 2 типу (ДМ) тільки призвело до зменшення частоти нефропатії, при цьому не знижується частота ретинопатії та макросудинних ускладнень. Результати другого масштабного дослідження ACCORD показали, що суворий контроль глікемії призвело до збільшення смертності серед пацієнтів, які страждають діабетом 2 типу.
У дослідженні UKPDS не було надійного ефекту суворого глікологічного контролю на інфаркті міокарда. Перспективним напрямком є підхід на основі припущення, що гіперглікемія має довгостроковий руйнівний ефект в обох типах 1 і цукровому діабеті 2 типу, і що суворий контроль глікоми, якщо не передбачено на дуже ранні стадії захворювання, недостатньо для повного запобігання ускладнень.
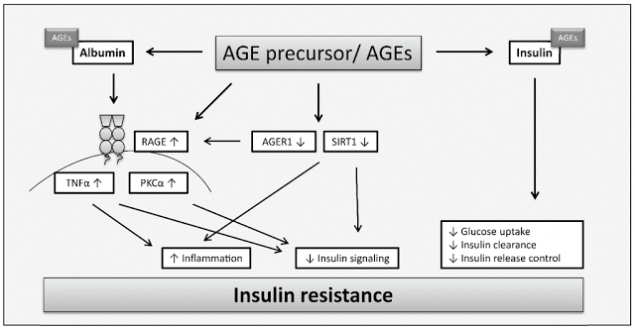
Ця гіпотеза ґрунтується на ідеї явища метаболічної пам'яті.Ранній глікемічний фон є «запаленим» в тканинах і органах призначення (тобто сітківки, нирки, серце, периферичні нерви). Перші дані, що підтверджують наявність метаболічної пам'яті, були отримані в дослідженнях тварин ретинальних клітин собак, одна група яких передається на суворий контроль глікемії через два місяці, а інший після 2,5-річного періоду гіперглікемії.
Сітківка було обстежено 5 років після початку експерименту. Парадоксально, тварини, які розпочали контроль глікемії після 2 місяців показали незначні докази ретинопатії, як і тварини з контролем глікемії протягом усього періоду дослідження. У той же час, у собак, які перенесли на суворий контроль глікемії після 2,5 років, частота ретинопатії була схожа на рівень ретинопатії собак, які перебували в стані гіперглікії протягом усього 5 років.
Термінова метаболічна пам'ять має кілька синонімів. Глікемічна пам'ять, гіперглікемічна пам'ять, спадковий ефект тощо. Клінічне підтвердження явища метаболічної пам'яті було отримано при широкомасштабному клінічному дослідженні цукрового діабету 1 типу (Діабети Ускладнення та контрольне випробування) та подальшому дослідженні EDIC (Епідеміологія інтерввенцій діабету та ускладнень). Під час постійного струму хворі з цукровим діабетом типу 1 діляться на 2 групи – інтенсивна інсулінотерапія та традиційна терапія, спрямована на нормалізацію глікемії.
Згодом EDIC дослідження, проведене на тій же популяції хворого, виявило, що серед учасників, які отримали стандартну терапію при ДКТ, поширеність мікросудинних ускладнень, таких як нефропатія і ретинопатія, вища порівняно з пацієнтами групи інтенсивної терапії, хоча після 6,5 років всі учасники дослідження перенесли на інтенсивну терапію.
Ще одним цікавим фактом є те, що в обох групах середній рівень глікованого гемоглобіну практично еквівалентний. Крім того, останніми EDIC знахідками підтримують довгостроковий вплив раннього глікологічного контролю на прогресування макросудинних ускладнень і серцево-судинних захворювань.
Метаболічна пам'ять також була виявлена у цукровому діабеті типу 2 у UKPDS (U.K. Перспективні дослідження діабету). Пацієнти з цукровим діабетом 2 типу, які перебували на стандартній терапії під час дослідження, мали вищі показники мікросудинних та серцево-судинних ускладнень порівняно з пацієнтами, які отримували інтенсивну допомогу.
Пошкодження впливу гіперглікемії на клітинний рівень здійснюється через чотири відомі механізми.: індукція поліолу шляху, реалізованої за допомогою ферменту альдосоредукази; збільшення утворення кінцевих продуктів надлишок глікозину (АГ); активація протеїнкінази C; активація шексоамінного шляху.
Значне значення кожного з цих механізмів було неодноразово підтверджено у дослідженнях тварин з використанням різних інгібіторів конкретної шляхи біохімічних реакцій, які перешкоджають діабетичних ускладнень. Однак проблема в тому, що, незважаючи на очевидний успіх застосування інгібіторів в експериментах тварин, при використанні тих же препаратів при лікуванні хворих, результати були надзвичайно незадоволеними.
Подальші дослідження виявили, що всі чотири патологічні реакції запускаються у відповідь на збільшення виробництва надоксидної аніції в мітохондріальній респіраторній мережі, процес індукованої гіперглікемією. Формування надоксиду відбувається під впливом підвищеної внутрішньоклітинної концентрації глюкози, порушення компонентів дихальної ланцюга мітохондрії та передачі електронів до молекули кисню.
Якщо генерація великої кількості надоксидної аніони є ключовим процесом розвитку діабетичних ускладнень, як важливо це в явищі метаболічної пам'яті? Супероксид, як і більшість реактивних молекул (радіки), має дуже коротку половину життя – не більше хвилин, тоді як глікомічна пам'ять може тривати протягом декількох років.
По суті, цілі для іонів супероксиду та інших радикалів є нуклеїновими кислотами, білками, ліпідами та ліпопротеїнами з тривалим періодом напіввиведення. Ці молекули, пошкоджені радикалами, можуть порушити роботу клітин протягом тривалого часу.
З'єднання 3-нітрозина, продукт взаємодії вільних радикалів з клітинними білками, може слугувати важливим маркером окислювального стресу при ускладненнях цукрового діабету. Ця речовина була використана в численних експериментах у моделях тварин, де продемонстровано роль окислювального стресу у формуванні глікоземної пам'яті.
Наприклад, Р.А. Ковлуру та ін. виявили, що у щурів з стрептоцитін-індукованим цукровим діабетом, нормалізацією рівня глікемії протягом 6 місяців після 6-місячного періоду гіперглікемії не призводять до значного зниження 3-х нітрозинових рівнів в ретинальних клітинах, оскільки тварин, в яких підтримувалася гіперглікемія. Я хотів би знову привернути увагу – нічого не змінилося протягом півроку, і це в щурі!
Потоки AGE - субстрат метаболічної пам'яті.
Разом з окислювальним стресом мітохондрію клітин підлягають іншому негативному впливу гіперглікемії - глікації мітохондріальних білків.й Зокрема, рівень метилгліоксалу, високоактивний побічний продукт гліколізу, знайдений для підвищеної ефективності у хворих на цукровий діабет.
Метилгліоксал, реагує білками і нуклеїновими кислотами клітинки, формує так звані кінцеві продукти надлишок глікозину - передові глікоцитаційні кінцеві продукти (AGE). Продукти AGE відіграють ключову роль у розвитку діабетичних ускладнень.
Глікація протеїнів мітохондріальної респіраторної ланцюга призводить до порушення її функціонування та обслуговування утворення надоксидних іонів незалежно від рівня глікемії. Крім того, формування продуктів AGE в структурі мітохондрії, будучи незворотним процесом, також може пояснити тривалий час існування метаболічної пам'яті.
Наведено, що у хворих на цукровий діабет рівень продуктів AGE у тканинах підвищується порівняно з здоровими людьми. Крім того, у пацієнтів з цукровим діабетом без ускладнень рівень продуктів AGE збільшений на 20-30%, а в цукровому діабеті, поєднані з серцево-судинними ускладненнями або мікроальбомінурії, на 40-100% порівняно з здоровими людьми.
У ЕДІКОМУ дослідженні рівень продуктів AGE, визначених біопсією шкіри, значно корелюється з поширеністю ретинопатії та нефропатії. На відміну від глікованого гемоглобіну, який проходить часткове ферментативне деглікозування при зниженні глікемії, рівень інших продуктів AGE не залежить від поточного рівня глюкози.
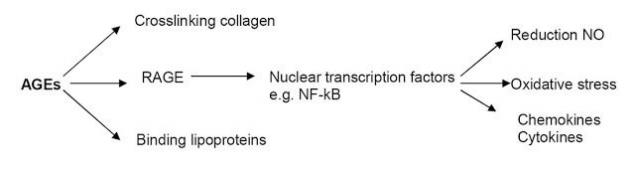
Крім безпосередньої участі AGE-продуктів, їх рецептори грають роль у формуванні метаболічної пам'яті, зокрема, типу рецептора, відомий як RAGE, що належить до надсімою імуноглобулінів молекул поверхневих клітин.
Прив'язка AGE і цей рецептор веде до утворення реактивних видів кисню (ROS), з подальшою активацією окислення-чутливого транскрипційного фактора NF-κB в судинній стіні, що регулює експресію запальних і «пошкоджених» генів, а сам ген RAGE.
Ці події в кінцевому підсумку призводять до ендотеліальної дисфункції і, в результаті до судинозвуження, запальних явищ, потовщення базальної мембрани і зниження здатності вазодилата. Негативний ефект АГ продукції реалізується не тільки в стінках судин, але і в неврозах і навіть в кістковій тканині. У нейронах продукти AGE спровокують поступове руйнування нервових волокон. Глікат мітохондріальних респіраторних білків в поєднанні з пошкодженням мітохондріальної ДНК може призвести до утворення нових поколінь ROS, стійких окислювальних стресів і пошкодження клітин.
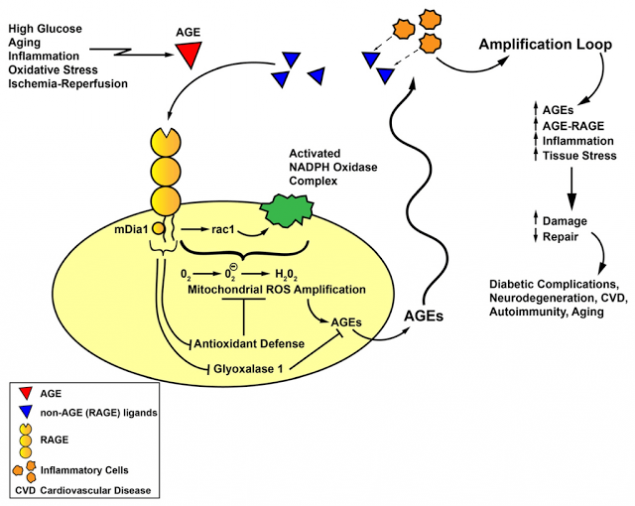
Злий коло: AGE-RAGE-інфламація-стрес.
Цей самодостатній процес підлягає метаболічної пам'яті, провідний механізм патогенезу діабетичних ускладнень, що є незалежно від рівня глікозії.й У зв'язку з цим методи «змикання» метаболічної пам'яті дуже перспективні з точки зору запобігання розвитку ускладнень.
По-перше, високі сподівання були розміщені на використанні антиоксидантів, оскільки окислювальний стрес відіграє ключову роль в механізмі пошкодження, але клінічне використання цих препаратів в цукровому діабеті не призвело до суттєвих поліпшень. Однак передбачається, що пригнічення утворення продуктів АГ, експресії РАГ та окислювального стресу у поєднанні з нормалізаціям рівня глікозії ефективно у запобіганні ускладнень.
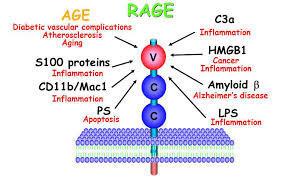
AGEs також може порушувати функцію клітин, пов'язуючи різні рецептори, включаючи макрофагії, ендотеліальні і гладкі м'язові клітини, клітини в тканині нирок і нервових клітинах. Ці рецептори, які взаємодіють з кінцевими продуктами, називають рецептори RAGE. Рецептори RAGE є ключовими медіаторами у відповідь організму на бактерії та віруси.
Гендери, глікозильні білки, ліпіди та навіть нуклеїнові кислоти можуть діяти як ліганці, які взаємодіють з рецепторами RAGE та ініціювати внутрішньоклітинні сигнали: наприклад, активація NF-kB, головний запальний агент, який сприяє старінню.
Замість прикріплення безпосередньо до білків, таких як колаген або еластин, ці розчинні AGE виступають в якості лігандів на рецепторів RAGE і провокують запальний процес. Рецептори RAGE зберігають клітинку в активному стані, що викликає короткочасні протизапальні реакції, щоб стати тривалою дисфункцією клітин.
Підводи AGE та їх рецептор (RAGE): від суден до Альцгеймера.
Рецептор глікозину кінцевого продукту (RAGE) є багатолігандом типу I трансмembrane глікопротеїну, що належить до імуноглобуліну (Ig) суперфаміливо. RAGE може бути залучений до ряду патологічних процесів, включаючи цукровий діабет, хвороба Альцгеймера (AD), системний амілоїдоз, пухлинний ріст.
РАГ спочатку характеризується своєю здатністю зв'язати АГ, приводи, утворені неезиматичними глікозиляціями і окисленням білків і ліпідів. Цей процес виникає в процесі нормального старіння і різко прискорюється в цукровому діабеті, де гіперглікемія слугує основним тригером. Свідчення субстанцій підтримує роль взаємодії AGE/RAGE в патофізиці діабету. У цукровому діабеті в судинах, моноцитах і подоцитах підростають обидва AGE та RAGE.
RAGE також може засвідчити фізіологічні функції, такі як нейронний ріст, виживання і регенерація, і відіграє важливу роль у прозапальних реакціях. RAGE виражається на високому рівні при розробці, особливо в центральній нервовій системі (CNS). Виражається також на нижній рівень у клітинах дорослого тіла: ендотелієві клітини, в тому числі гладкі м'язові клітини, в мононуклеючі фагоцити, перикітети, нейрони, кардіоміоцити, гепатоцити. Компанія RAGE ligands включає в себе глікозинні кінцеві продукти (AGEs), амілоїдно-β протеїну (Aβ), HMG-1 (також відомий як ампгарін), а також кілька членів білка S100.
Блокада активації RAGE з рекомбінантним sRAGE або функціонально-блокуючим антитілам зменшує рухливість судин, розвиток атеросклеротичного ураження, а також посилює загоєння ран при діабетичних грижах. RAGE-zero diabetic мишей не розвиває ознаки нефропатії, в тому числі збільшення розширення мезанальної матриці і потовщення гломеруальної мембрани.
Безперечно, трансгенна гіперекпресія RAGE призводить до загострення діабетичної нефропатії і ретинопатії. RAGE також є рецептором для β-збиткових фібрилів, конструкцій, які характерні для амілоїдів. Aβ – головний компонент нейродегенеративних нальотів, пов’язаних з хворобою Альцгеймера (AD), а також RAGE колокалізовані з Aβ в мозку хворих AD у підвищених розмірах.
 р.
р.
З молекулярної точки зору хвороба Альцгеймера характеризується відкладеннями аномально агрегованих білків. У разі позаклітинних амілоїдних нальотів такі родовища переважно складаються з ниток β-амілоїдних пептидів (Аβ), а в разі внутрішньоклітинних нейрофібрилярних трикутників (НФТ), переважно з протеїну тау.
AD також характеризується підвищеним виразом RAGE в нейронах. RAGE є рецептором сімейства імуноглобулінів, який має багато лігандів, які функції як сигналізатор Aβ на поверхні клітин. Glycosylation End Product Receptor (RAGE), який локалізований не тільки на нейронах, астрогліа і мікрогліа, але і на ендотеліальних клітинах, де він виступає транспортером амілоїдної бета до мозку з кровоплину.
Кілька груп показали, що настій Aβ40 в мишей призводить до судинозвуження судин головного мозку і ослабленого церебрального кровообігу (CBF). Пацієнти, які страждають від АД, також ослаблюють церебральний кровообіг. У моделях АД, в яких трансгенних тварин перевизнають амілоїдний прекурсорний білок (APP), що призводить до захворювання, що викликає утворення нальотів, RAGE було показано, щоб бути залученим як патогенний фактор при прогресуванні захворювання.
RAGE було показано для зв'язування Aβ-пептидів. Пригнічення такої взаємодії гальмує накопичення β в трансгенних тваринах в моделі; отже, вважається, що RAGE бере участь в AD. Лікування за допомогою sRAGE (розчинний RAGE), а також антитіла анти-RAGE було показано для зменшення кількості нальотів (Деан та ін, 2003). Блокування взаємодії РАГ з амілоїдом з антитілами може бути підходящим способом лікування хворих з АД; однак існуючі поліклональні антитіла, отримані з сироватки тварин не підходять для хронічного лікування людини. Видання
Автор: Андрій Білловкін
Читати далі:
Антипаразитичне очищення і саджанці
Ви можете лікувати нервову систему і гіпертонічну хворобу і отримати інсульт через ostechondrosis!
P.S. І пам'ятайте, що просто змініть наше споживання – разом ми змінюємо світ!
Приєднуйтесь до нас на Facebook, VKontakte, Odnoklassniki
Джерело: www.beloveshkin.com/2016/05/glikirovanie-i-metabolicheskaya-pamyat-mest-podaetsya-kholodnoj.html
Гляка довголічених білків і ДНК - це процес, який невидимий спочатку, але дуже важко ремонтувати пізніше. Так, глікозинні кінцеві продукти дуже вироковані, а помста - це блюдо, подається холодним.

Що таке метаболічна пам'ять?
У дослідженні цукрового діабету з'явився термін «метаболічна пам'ять». Справа в тому, що, незважаючи на досягнення в лікуванні захворювання - розвиток нових цукрово-жовтих агентів, досягнення успішного контролю глікемії і визначення маркерів глікемії, більшість пацієнтів розвиваються серйозні ураження органів призначення, що призводять до серйозних ускладнень.
Метаболічна пам'ять (відоме як гіперглікемічна або судинна пам'ять) є ефектом, що призводить до розвитку довгострокових ефектів тривалого періоду погано компенсованого рівня глюкози крові. Іншими словами, довший цукровий діабет залишається некомпенсованим, чим довше цей шкідливий ефект зберігається, навіть після кращого контролю захворювання.
Спочатку ранні епізоди гіперглікемії негативно впливають на рівень ретинальних клітин, нирок, а також функціонування нервових волокон. «Метаболічна пам'ять» – це ситуація, де збільшення глікемії – навіть перед постановкою діагнозу захворювання – вже патологічно впливає на різні системи організму.Особливо на нервових волокнах. Більш того, якщо глікозний контроль був недостатнім протягом тривалого часу, ефект пошкодження може зберігатися в майбутньому, навіть після оптимізації рівня глюкози.
Зокрема, у великому дослідженні АДВАНС було виявлено, що суворий контроль глікемії у цукровому діабеті 2 типу (ДМ) тільки призвело до зменшення частоти нефропатії, при цьому не знижується частота ретинопатії та макросудинних ускладнень. Результати другого масштабного дослідження ACCORD показали, що суворий контроль глікемії призвело до збільшення смертності серед пацієнтів, які страждають діабетом 2 типу.
У дослідженні UKPDS не було надійного ефекту суворого глікологічного контролю на інфаркті міокарда. Перспективним напрямком є підхід на основі припущення, що гіперглікемія має довгостроковий руйнівний ефект в обох типах 1 і цукровому діабеті 2 типу, і що суворий контроль глікоми, якщо не передбачено на дуже ранні стадії захворювання, недостатньо для повного запобігання ускладнень.

Ця гіпотеза ґрунтується на ідеї явища метаболічної пам'яті.Ранній глікемічний фон є «запаленим» в тканинах і органах призначення (тобто сітківки, нирки, серце, периферичні нерви). Перші дані, що підтверджують наявність метаболічної пам'яті, були отримані в дослідженнях тварин ретинальних клітин собак, одна група яких передається на суворий контроль глікемії через два місяці, а інший після 2,5-річного періоду гіперглікемії.
Сітківка було обстежено 5 років після початку експерименту. Парадоксально, тварини, які розпочали контроль глікемії після 2 місяців показали незначні докази ретинопатії, як і тварини з контролем глікемії протягом усього періоду дослідження. У той же час, у собак, які перенесли на суворий контроль глікемії після 2,5 років, частота ретинопатії була схожа на рівень ретинопатії собак, які перебували в стані гіперглікії протягом усього 5 років.
Термінова метаболічна пам'ять має кілька синонімів. Глікемічна пам'ять, гіперглікемічна пам'ять, спадковий ефект тощо. Клінічне підтвердження явища метаболічної пам'яті було отримано при широкомасштабному клінічному дослідженні цукрового діабету 1 типу (Діабети Ускладнення та контрольне випробування) та подальшому дослідженні EDIC (Епідеміологія інтерввенцій діабету та ускладнень). Під час постійного струму хворі з цукровим діабетом типу 1 діляться на 2 групи – інтенсивна інсулінотерапія та традиційна терапія, спрямована на нормалізацію глікемії.
Згодом EDIC дослідження, проведене на тій же популяції хворого, виявило, що серед учасників, які отримали стандартну терапію при ДКТ, поширеність мікросудинних ускладнень, таких як нефропатія і ретинопатія, вища порівняно з пацієнтами групи інтенсивної терапії, хоча після 6,5 років всі учасники дослідження перенесли на інтенсивну терапію.
Ще одним цікавим фактом є те, що в обох групах середній рівень глікованого гемоглобіну практично еквівалентний. Крім того, останніми EDIC знахідками підтримують довгостроковий вплив раннього глікологічного контролю на прогресування макросудинних ускладнень і серцево-судинних захворювань.
Метаболічна пам'ять також була виявлена у цукровому діабеті типу 2 у UKPDS (U.K. Перспективні дослідження діабету). Пацієнти з цукровим діабетом 2 типу, які перебували на стандартній терапії під час дослідження, мали вищі показники мікросудинних та серцево-судинних ускладнень порівняно з пацієнтами, які отримували інтенсивну допомогу.
Пошкодження впливу гіперглікемії на клітинний рівень здійснюється через чотири відомі механізми.: індукція поліолу шляху, реалізованої за допомогою ферменту альдосоредукази; збільшення утворення кінцевих продуктів надлишок глікозину (АГ); активація протеїнкінази C; активація шексоамінного шляху.
Значне значення кожного з цих механізмів було неодноразово підтверджено у дослідженнях тварин з використанням різних інгібіторів конкретної шляхи біохімічних реакцій, які перешкоджають діабетичних ускладнень. Однак проблема в тому, що, незважаючи на очевидний успіх застосування інгібіторів в експериментах тварин, при використанні тих же препаратів при лікуванні хворих, результати були надзвичайно незадоволеними.
Подальші дослідження виявили, що всі чотири патологічні реакції запускаються у відповідь на збільшення виробництва надоксидної аніції в мітохондріальній респіраторній мережі, процес індукованої гіперглікемією. Формування надоксиду відбувається під впливом підвищеної внутрішньоклітинної концентрації глюкози, порушення компонентів дихальної ланцюга мітохондрії та передачі електронів до молекули кисню.
Якщо генерація великої кількості надоксидної аніони є ключовим процесом розвитку діабетичних ускладнень, як важливо це в явищі метаболічної пам'яті? Супероксид, як і більшість реактивних молекул (радіки), має дуже коротку половину життя – не більше хвилин, тоді як глікомічна пам'ять може тривати протягом декількох років.
По суті, цілі для іонів супероксиду та інших радикалів є нуклеїновими кислотами, білками, ліпідами та ліпопротеїнами з тривалим періодом напіввиведення. Ці молекули, пошкоджені радикалами, можуть порушити роботу клітин протягом тривалого часу.
З'єднання 3-нітрозина, продукт взаємодії вільних радикалів з клітинними білками, може слугувати важливим маркером окислювального стресу при ускладненнях цукрового діабету. Ця речовина була використана в численних експериментах у моделях тварин, де продемонстровано роль окислювального стресу у формуванні глікоземної пам'яті.
Наприклад, Р.А. Ковлуру та ін. виявили, що у щурів з стрептоцитін-індукованим цукровим діабетом, нормалізацією рівня глікемії протягом 6 місяців після 6-місячного періоду гіперглікемії не призводять до значного зниження 3-х нітрозинових рівнів в ретинальних клітинах, оскільки тварин, в яких підтримувалася гіперглікемія. Я хотів би знову привернути увагу – нічого не змінилося протягом півроку, і це в щурі!
Потоки AGE - субстрат метаболічної пам'яті.
Разом з окислювальним стресом мітохондрію клітин підлягають іншому негативному впливу гіперглікемії - глікації мітохондріальних білків.й Зокрема, рівень метилгліоксалу, високоактивний побічний продукт гліколізу, знайдений для підвищеної ефективності у хворих на цукровий діабет.
Метилгліоксал, реагує білками і нуклеїновими кислотами клітинки, формує так звані кінцеві продукти надлишок глікозину - передові глікоцитаційні кінцеві продукти (AGE). Продукти AGE відіграють ключову роль у розвитку діабетичних ускладнень.
Глікація протеїнів мітохондріальної респіраторної ланцюга призводить до порушення її функціонування та обслуговування утворення надоксидних іонів незалежно від рівня глікемії. Крім того, формування продуктів AGE в структурі мітохондрії, будучи незворотним процесом, також може пояснити тривалий час існування метаболічної пам'яті.

Наведено, що у хворих на цукровий діабет рівень продуктів AGE у тканинах підвищується порівняно з здоровими людьми. Крім того, у пацієнтів з цукровим діабетом без ускладнень рівень продуктів AGE збільшений на 20-30%, а в цукровому діабеті, поєднані з серцево-судинними ускладненнями або мікроальбомінурії, на 40-100% порівняно з здоровими людьми.
У ЕДІКОМУ дослідженні рівень продуктів AGE, визначених біопсією шкіри, значно корелюється з поширеністю ретинопатії та нефропатії. На відміну від глікованого гемоглобіну, який проходить часткове ферментативне деглікозування при зниженні глікемії, рівень інших продуктів AGE не залежить від поточного рівня глюкози.
Крім безпосередньої участі AGE-продуктів, їх рецептори грають роль у формуванні метаболічної пам'яті, зокрема, типу рецептора, відомий як RAGE, що належить до надсімою імуноглобулінів молекул поверхневих клітин.
Прив'язка AGE і цей рецептор веде до утворення реактивних видів кисню (ROS), з подальшою активацією окислення-чутливого транскрипційного фактора NF-κB в судинній стіні, що регулює експресію запальних і «пошкоджених» генів, а сам ген RAGE.
Ці події в кінцевому підсумку призводять до ендотеліальної дисфункції і, в результаті до судинозвуження, запальних явищ, потовщення базальної мембрани і зниження здатності вазодилата. Негативний ефект АГ продукції реалізується не тільки в стінках судин, але і в неврозах і навіть в кістковій тканині. У нейронах продукти AGE спровокують поступове руйнування нервових волокон. Глікат мітохондріальних респіраторних білків в поєднанні з пошкодженням мітохондріальної ДНК може призвести до утворення нових поколінь ROS, стійких окислювальних стресів і пошкодження клітин.

Злий коло: AGE-RAGE-інфламація-стрес.
Цей самодостатній процес підлягає метаболічної пам'яті, провідний механізм патогенезу діабетичних ускладнень, що є незалежно від рівня глікозії.й У зв'язку з цим методи «змикання» метаболічної пам'яті дуже перспективні з точки зору запобігання розвитку ускладнень.
По-перше, високі сподівання були розміщені на використанні антиоксидантів, оскільки окислювальний стрес відіграє ключову роль в механізмі пошкодження, але клінічне використання цих препаратів в цукровому діабеті не призвело до суттєвих поліпшень. Однак передбачається, що пригнічення утворення продуктів АГ, експресії РАГ та окислювального стресу у поєднанні з нормалізаціям рівня глікозії ефективно у запобіганні ускладнень.

AGEs також може порушувати функцію клітин, пов'язуючи різні рецептори, включаючи макрофагії, ендотеліальні і гладкі м'язові клітини, клітини в тканині нирок і нервових клітинах. Ці рецептори, які взаємодіють з кінцевими продуктами, називають рецептори RAGE. Рецептори RAGE є ключовими медіаторами у відповідь організму на бактерії та віруси.
Гендери, глікозильні білки, ліпіди та навіть нуклеїнові кислоти можуть діяти як ліганці, які взаємодіють з рецепторами RAGE та ініціювати внутрішньоклітинні сигнали: наприклад, активація NF-kB, головний запальний агент, який сприяє старінню.
Замість прикріплення безпосередньо до білків, таких як колаген або еластин, ці розчинні AGE виступають в якості лігандів на рецепторів RAGE і провокують запальний процес. Рецептори RAGE зберігають клітинку в активному стані, що викликає короткочасні протизапальні реакції, щоб стати тривалою дисфункцією клітин.
Підводи AGE та їх рецептор (RAGE): від суден до Альцгеймера.
Рецептор глікозину кінцевого продукту (RAGE) є багатолігандом типу I трансмembrane глікопротеїну, що належить до імуноглобуліну (Ig) суперфаміливо. RAGE може бути залучений до ряду патологічних процесів, включаючи цукровий діабет, хвороба Альцгеймера (AD), системний амілоїдоз, пухлинний ріст.
РАГ спочатку характеризується своєю здатністю зв'язати АГ, приводи, утворені неезиматичними глікозиляціями і окисленням білків і ліпідів. Цей процес виникає в процесі нормального старіння і різко прискорюється в цукровому діабеті, де гіперглікемія слугує основним тригером. Свідчення субстанцій підтримує роль взаємодії AGE/RAGE в патофізиці діабету. У цукровому діабеті в судинах, моноцитах і подоцитах підростають обидва AGE та RAGE.
RAGE також може засвідчити фізіологічні функції, такі як нейронний ріст, виживання і регенерація, і відіграє важливу роль у прозапальних реакціях. RAGE виражається на високому рівні при розробці, особливо в центральній нервовій системі (CNS). Виражається також на нижній рівень у клітинах дорослого тіла: ендотелієві клітини, в тому числі гладкі м'язові клітини, в мононуклеючі фагоцити, перикітети, нейрони, кардіоміоцити, гепатоцити. Компанія RAGE ligands включає в себе глікозинні кінцеві продукти (AGEs), амілоїдно-β протеїну (Aβ), HMG-1 (також відомий як ампгарін), а також кілька членів білка S100.
Блокада активації RAGE з рекомбінантним sRAGE або функціонально-блокуючим антитілам зменшує рухливість судин, розвиток атеросклеротичного ураження, а також посилює загоєння ран при діабетичних грижах. RAGE-zero diabetic мишей не розвиває ознаки нефропатії, в тому числі збільшення розширення мезанальної матриці і потовщення гломеруальної мембрани.
Безперечно, трансгенна гіперекпресія RAGE призводить до загострення діабетичної нефропатії і ретинопатії. RAGE також є рецептором для β-збиткових фібрилів, конструкцій, які характерні для амілоїдів. Aβ – головний компонент нейродегенеративних нальотів, пов’язаних з хворобою Альцгеймера (AD), а також RAGE колокалізовані з Aβ в мозку хворих AD у підвищених розмірах.
 р.
р.З молекулярної точки зору хвороба Альцгеймера характеризується відкладеннями аномально агрегованих білків. У разі позаклітинних амілоїдних нальотів такі родовища переважно складаються з ниток β-амілоїдних пептидів (Аβ), а в разі внутрішньоклітинних нейрофібрилярних трикутників (НФТ), переважно з протеїну тау.
AD також характеризується підвищеним виразом RAGE в нейронах. RAGE є рецептором сімейства імуноглобулінів, який має багато лігандів, які функції як сигналізатор Aβ на поверхні клітин. Glycosylation End Product Receptor (RAGE), який локалізований не тільки на нейронах, астрогліа і мікрогліа, але і на ендотеліальних клітинах, де він виступає транспортером амілоїдної бета до мозку з кровоплину.
Кілька груп показали, що настій Aβ40 в мишей призводить до судинозвуження судин головного мозку і ослабленого церебрального кровообігу (CBF). Пацієнти, які страждають від АД, також ослаблюють церебральний кровообіг. У моделях АД, в яких трансгенних тварин перевизнають амілоїдний прекурсорний білок (APP), що призводить до захворювання, що викликає утворення нальотів, RAGE було показано, щоб бути залученим як патогенний фактор при прогресуванні захворювання.
RAGE було показано для зв'язування Aβ-пептидів. Пригнічення такої взаємодії гальмує накопичення β в трансгенних тваринах в моделі; отже, вважається, що RAGE бере участь в AD. Лікування за допомогою sRAGE (розчинний RAGE), а також антитіла анти-RAGE було показано для зменшення кількості нальотів (Деан та ін, 2003). Блокування взаємодії РАГ з амілоїдом з антитілами може бути підходящим способом лікування хворих з АД; однак існуючі поліклональні антитіла, отримані з сироватки тварин не підходять для хронічного лікування людини. Видання
Автор: Андрій Білловкін
Читати далі:
Антипаразитичне очищення і саджанці
Ви можете лікувати нервову систему і гіпертонічну хворобу і отримати інсульт через ostechondrosis!
P.S. І пам'ятайте, що просто змініть наше споживання – разом ми змінюємо світ!
Приєднуйтесь до нас на Facebook, VKontakte, Odnoklassniki
Джерело: www.beloveshkin.com/2016/05/glikirovanie-i-metabolicheskaya-pamyat-mest-podaetsya-kholodnoj.html