528
Чи працює наша смерть?
У 1881 році німецький біолог Август Вайсманн дав лекцію в Фрібурзі на довголіття життя. «Я не вважаю смерті як основну необхідність, але як щось набуте вдруге, як адаптація», – зловживаю, яка циркулюється в багатьох наукових виданнях і була широко обговорена в провідних газетах часу. 
академік російської академії наук, директор Інституту фізико-хімічної біології імені А. Н. Білозерського Московського державного університету, фахівець з механізмів біологічного окислення, в тому числі на мембранах мітохондріалу. Він працює над «притомою для старшого віку». Має найвищий індекс цитування серед усіх російських біологів.
За словами Вейсмана, жива природа придумала в процесі еволюції спеціальну програму, яка поступово вбиває старі організми, тим самим очищаючи спосіб молоді. Автор негайно звинуватив анти-Darwinism, а його гіпотеза була розірвана як розумна спроба видалити похилого керівника відділу, де працював Weisman. Наприкінці свого життя він припинив цитувати свою ідею смерті як адаптації, а потім покинути його
Тим не менш, ідея старіння і смерті від старого віку в результаті певної програми, властивої життєдіяльності, все ще має її прихильники. Більш того, за останні роки, нові докази були обраховані на користь дійсності концепції Вейсмана. Це в першу чергу відкриття апоптозу - смерть клітинного запрограмованого в його геному, і існування аналогічної програми в одноклітинному, де збігаються поняття «клітину» і «організм».
22 травня 2015 року в журналі «Наукові звіти» з’явилася стаття J.I. Гайаші та його одинадцять співавторів в Університеті Цукуба в Японії під назвою «Епігенетичне регулювання ядерних генів ГКАТ та ШМТ2 викликає респіраторні дефекти в мітохондрії людини у старінні». Автори стверджують, що мітохондрія в клітинах людей більше 80 страждають від повторного уповільнення дихання, і цей серйозний дефект викликаний не накопиченням випадкових мутацій в ДНК, але при епігенетичному регуляції роботи всього декількох генів. Важливо, що автори вдалося виправити цей дефект у певній мірі, тобто як омолодити старі клітини. (Ас І. П. Павлов, істинний лікар-фізіолог може вважатися тільки тим, хто повернувся до нормального порушеного фізіологічного процесу.)
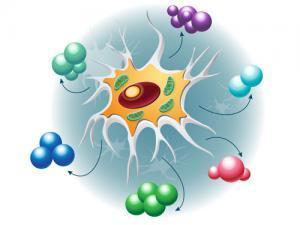
Фібробласти - це клітини сполучної тканини тіла. Найбільша тканина «прості» з точки зору біолога. Ці клітини легко культуруються поза тілом, тому вони часто використовуються в експериментах. У цьому експерименті вони омолодилися.
Гіпотез Stochastic Aging пропонує, що ми вікові і штамповані, оскільки випадкові пошкодження накопичуються в клітинах.
По-перше, Гайаші та його колеги вимірювали дихання ізольованих фібробластних клітин, отриманих з ембріонів людини або дітей з шести місяців до 12 років і з важко літніх людей (80 до 97 років). Виявилося, що дихання клітин в 97-річному віці в шість разів нижче, ніж в ембріоні або молоді люди, і ця патологія розвивається в основному через 80 років (в 80-річному подиханні було зменшено проти молодого менше половини). Потім з 27958 генів генів геному людини, 371 генів, пов’язаних з мітохондріальним диханням та перекладом, і серед них вибрали шість генів, які змінилися з віком (закінчення літературними даними) більш ніж на півтора рази.
Три з шести генів не залежали в фібробластах двох груп, які навчалися, ще було стимулювати в похилому, а решта двох були гальмовані. Цей пригнічення може бути викликаний випадковою мутацією в ДНК відповідних генів, якщо сточна гіпотеза старіння є правильним в результаті пошкодження молекул ДНК з віком.
Ще однією можливістю було те, що старіння викликається спеціальною біологічною програмою, яка контролює діяльність певних генів без їх незворотного пошкодження мутацій. Контролюючі програми такого роду визначаються роботою спеціальних білків-назимів, присутніх в хромосомах (так званих епігенетичних програм).

Мітохондрія в клітинах людей понад 80 страждають від повторного уповільнення дихання, і цей дефект не викликається накопиченням випадкових мутацій. Щоб вибрати між цими двома варіантами, японські автори використовуються наступні техніки. Зіркиковські фібробласти були запрограмовані: вони перетворилися в стовбурові клітини, з яких потім переросли фібробласти. Якщо це була мутація ДНК, це процедура не може допомогти: як стовбурові клітини, так і запрограмовані фібробласти, отримані з них, все ще містять мутантну ДНК і тому страждають від мутації індукованої дихальної гальмування. Якщо це не генетична, але епігенетика, то було серйозним шансом виправити респіраторний дефект при переході «фібробласт – стовбурові клітини – новий фібробласт». Справа в тому, що трансформація фібробласту в стовбурову клітину переновлює клітинну лінію, яка, як це було, обтяжує тягар епігенетичного регулювання всього попереднього життя.
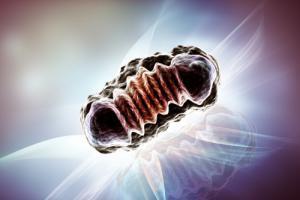
Мітохондрія - енергетична станція клітини. Ми пам'ятаємо цей метафор зі школи. Невеликий органель у вигляді сфери або еліпсу з двома мембранами. Оксидування поживних речовин, що надходять в клітинку з киснем і через цей процес (горяння) генерує основні молекули енергії - ATP. Вважають, що мітохондрія походить від бактерій, які були всмоктовані і вимушені працювати для предків екуаріотів. Мітохондрія має скромний залишок геному, хоча більшість його генів перенесли в ядро хостових клітин мільярдів років тому.
Інформація РНК, це зематр РНК, або мРНК. Перевізник інформації з ДНК - головний репозиторій - до робочих машин клітини, рибосом і білками. Один з хромосомних генів скопійований на мРНК, а також інструкція з виробництва білків; потім перевозиться до цитоплазми клітини, де рибосоми роблять білки за цією інструкцією. Матриця РНК є такими генами, як гени (і ще більше), чому є так багато видів білків в клітинці.
Отже, автори вдалося практично повністю видалити вікові респіраторні гальмування старих фібробластів шляхом перепрограмування цих клітин. Потім подивилися два гени, які сповільнилися з віком. Однією з цих генів зустрілися очікування японських вчених. Це був ген GCAT фермент, необхідний для синтезу найпростішої амінокислоти, гліцину (NH+3-CH2-COO-). Кількість інформації РНК, що виробляється цим геном, знизилася багато разів з віком до донора фібробласту, і повністю вилучено це зниження. Після цього застосовано механізм «відхилення» цього специфічного гена РНК у молодих фібробластах, який пригнічує дихання. Штучне прискорення того ж гена в 97-річній людині частково відновило високу респіраторну норму (це курс потрійний). І, нарешті, досвід «під ключ»: За 10 днів у гліцино-багатому середовищі були культуровані 97-річні фібробласти. Їх дихання підвищило 2,5 рази.
Очевидно, що зниження частоти синтезу гліцину призвело до його дефіциту в клітині, і це, в свою чергу, пригнічує синтез гліцинових порфіринів (необхідний для утворення респіраторних ферментів), а також одного з основних клітинних антиоксидантів - глутаміл-цистеїл-гліцину (глютиція), гній, піримідинів, креатину та фібрилярних білків, таких як колаген, де гліцин робить 25% всіх амінокислот.
В цілому, робота Хайаші та його колег може бути підведена за такою схемою.
Програма старіння → епігенетична пригнічення гена GCAT → зниження синтезу гліцину в клітині → пригнічення дихання мітохондрій.
Залишилося незрозуміло, як працює програма старіння, а особливо як працює епігенетичний контроль гена GCAT. Намагатися якось уточнити структуру програми, поданих авторами, навряд чи можна вважати успішним. Є багато показань, що програма старіння передбачає реактивні види кисню, що утворюються в мітохондрії (супероксид, перекис водню, гідроксиль радикальний). Автори спробували вимірювати надоксид у фібробластах молодих і старих людей з використанням мітосокської катації як реагенту супероксиду. Вони виявили деяке збільшення відповіді на це реагент з віком (97-річному віці 67% більше відповідь, ніж ембріон). Тим не менш, мітосок вимірює два взаємопов'язані параметри одночасно: супероксид і мітохондріальний мембранний потенціал.
Незважаючи на свою оригінальність, робота під час обговорення повинна бути попередньою. Крім того, великий розсіювання даних Гайаші та його колег не дозволяють зробити остаточний висновок про рівень перекису. І тут ми повинні, на жаль, держава, яка, незважаючи на свою оригінальність, повинна бути розглянута як чисто попередня. Неважливо, що молоді люди мали лише три і один ембріон, і похилого лише чотири, і один з найбільшим ефектом старіння (старий пацієнт 97-річного віку) був також тільки в скутальному, а другий три були між 80 і 86 років. Не серйозний геронтологічний журнал прийматиме статтю, де експериментальні когорти так дрібні. Не краще повторювати: завжди були тільки три. Ключовий експеримент щодо дії гліцину додають до фібробластів, як правило, проводиться тільки в 97-річному віці, що у порівнянні з єдиним ембріоном. Не варто збігатися з тим, що це важливе спостереження поміщається в Додаток, а не в головному тексті статті.
На жаль, є інші дослідники, які повинні повторювати цю потенційно цікава робота.Видання
P.S. І пам'ятайте, що просто змініть наше споживання – разом ми змінюємо світ!
Приєднуйтесь до нас на Facebook і VKontakte, і ми також в Однокласниках
Джерело: kot.sh/statya/233/nasha-smert-zaprogrammirovana

академік російської академії наук, директор Інституту фізико-хімічної біології імені А. Н. Білозерського Московського державного університету, фахівець з механізмів біологічного окислення, в тому числі на мембранах мітохондріалу. Він працює над «притомою для старшого віку». Має найвищий індекс цитування серед усіх російських біологів.
За словами Вейсмана, жива природа придумала в процесі еволюції спеціальну програму, яка поступово вбиває старі організми, тим самим очищаючи спосіб молоді. Автор негайно звинуватив анти-Darwinism, а його гіпотеза була розірвана як розумна спроба видалити похилого керівника відділу, де працював Weisman. Наприкінці свого життя він припинив цитувати свою ідею смерті як адаптації, а потім покинути його
Тим не менш, ідея старіння і смерті від старого віку в результаті певної програми, властивої життєдіяльності, все ще має її прихильники. Більш того, за останні роки, нові докази були обраховані на користь дійсності концепції Вейсмана. Це в першу чергу відкриття апоптозу - смерть клітинного запрограмованого в його геному, і існування аналогічної програми в одноклітинному, де збігаються поняття «клітину» і «організм».
22 травня 2015 року в журналі «Наукові звіти» з’явилася стаття J.I. Гайаші та його одинадцять співавторів в Університеті Цукуба в Японії під назвою «Епігенетичне регулювання ядерних генів ГКАТ та ШМТ2 викликає респіраторні дефекти в мітохондрії людини у старінні». Автори стверджують, що мітохондрія в клітинах людей більше 80 страждають від повторного уповільнення дихання, і цей серйозний дефект викликаний не накопиченням випадкових мутацій в ДНК, але при епігенетичному регуляції роботи всього декількох генів. Важливо, що автори вдалося виправити цей дефект у певній мірі, тобто як омолодити старі клітини. (Ас І. П. Павлов, істинний лікар-фізіолог може вважатися тільки тим, хто повернувся до нормального порушеного фізіологічного процесу.)

Фібробласти - це клітини сполучної тканини тіла. Найбільша тканина «прості» з точки зору біолога. Ці клітини легко культуруються поза тілом, тому вони часто використовуються в експериментах. У цьому експерименті вони омолодилися.
Гіпотез Stochastic Aging пропонує, що ми вікові і штамповані, оскільки випадкові пошкодження накопичуються в клітинах.
По-перше, Гайаші та його колеги вимірювали дихання ізольованих фібробластних клітин, отриманих з ембріонів людини або дітей з шести місяців до 12 років і з важко літніх людей (80 до 97 років). Виявилося, що дихання клітин в 97-річному віці в шість разів нижче, ніж в ембріоні або молоді люди, і ця патологія розвивається в основному через 80 років (в 80-річному подиханні було зменшено проти молодого менше половини). Потім з 27958 генів генів геному людини, 371 генів, пов’язаних з мітохондріальним диханням та перекладом, і серед них вибрали шість генів, які змінилися з віком (закінчення літературними даними) більш ніж на півтора рази.
Три з шести генів не залежали в фібробластах двох груп, які навчалися, ще було стимулювати в похилому, а решта двох були гальмовані. Цей пригнічення може бути викликаний випадковою мутацією в ДНК відповідних генів, якщо сточна гіпотеза старіння є правильним в результаті пошкодження молекул ДНК з віком.
Ще однією можливістю було те, що старіння викликається спеціальною біологічною програмою, яка контролює діяльність певних генів без їх незворотного пошкодження мутацій. Контролюючі програми такого роду визначаються роботою спеціальних білків-назимів, присутніх в хромосомах (так званих епігенетичних програм).

Мітохондрія в клітинах людей понад 80 страждають від повторного уповільнення дихання, і цей дефект не викликається накопиченням випадкових мутацій. Щоб вибрати між цими двома варіантами, японські автори використовуються наступні техніки. Зіркиковські фібробласти були запрограмовані: вони перетворилися в стовбурові клітини, з яких потім переросли фібробласти. Якщо це була мутація ДНК, це процедура не може допомогти: як стовбурові клітини, так і запрограмовані фібробласти, отримані з них, все ще містять мутантну ДНК і тому страждають від мутації індукованої дихальної гальмування. Якщо це не генетична, але епігенетика, то було серйозним шансом виправити респіраторний дефект при переході «фібробласт – стовбурові клітини – новий фібробласт». Справа в тому, що трансформація фібробласту в стовбурову клітину переновлює клітинну лінію, яка, як це було, обтяжує тягар епігенетичного регулювання всього попереднього життя.

Мітохондрія - енергетична станція клітини. Ми пам'ятаємо цей метафор зі школи. Невеликий органель у вигляді сфери або еліпсу з двома мембранами. Оксидування поживних речовин, що надходять в клітинку з киснем і через цей процес (горяння) генерує основні молекули енергії - ATP. Вважають, що мітохондрія походить від бактерій, які були всмоктовані і вимушені працювати для предків екуаріотів. Мітохондрія має скромний залишок геному, хоча більшість його генів перенесли в ядро хостових клітин мільярдів років тому.
Інформація РНК, це зематр РНК, або мРНК. Перевізник інформації з ДНК - головний репозиторій - до робочих машин клітини, рибосом і білками. Один з хромосомних генів скопійований на мРНК, а також інструкція з виробництва білків; потім перевозиться до цитоплазми клітини, де рибосоми роблять білки за цією інструкцією. Матриця РНК є такими генами, як гени (і ще більше), чому є так багато видів білків в клітинці.
Отже, автори вдалося практично повністю видалити вікові респіраторні гальмування старих фібробластів шляхом перепрограмування цих клітин. Потім подивилися два гени, які сповільнилися з віком. Однією з цих генів зустрілися очікування японських вчених. Це був ген GCAT фермент, необхідний для синтезу найпростішої амінокислоти, гліцину (NH+3-CH2-COO-). Кількість інформації РНК, що виробляється цим геном, знизилася багато разів з віком до донора фібробласту, і повністю вилучено це зниження. Після цього застосовано механізм «відхилення» цього специфічного гена РНК у молодих фібробластах, який пригнічує дихання. Штучне прискорення того ж гена в 97-річній людині частково відновило високу респіраторну норму (це курс потрійний). І, нарешті, досвід «під ключ»: За 10 днів у гліцино-багатому середовищі були культуровані 97-річні фібробласти. Їх дихання підвищило 2,5 рази.
Очевидно, що зниження частоти синтезу гліцину призвело до його дефіциту в клітині, і це, в свою чергу, пригнічує синтез гліцинових порфіринів (необхідний для утворення респіраторних ферментів), а також одного з основних клітинних антиоксидантів - глутаміл-цистеїл-гліцину (глютиція), гній, піримідинів, креатину та фібрилярних білків, таких як колаген, де гліцин робить 25% всіх амінокислот.
В цілому, робота Хайаші та його колег може бути підведена за такою схемою.
Програма старіння → епігенетична пригнічення гена GCAT → зниження синтезу гліцину в клітині → пригнічення дихання мітохондрій.
Залишилося незрозуміло, як працює програма старіння, а особливо як працює епігенетичний контроль гена GCAT. Намагатися якось уточнити структуру програми, поданих авторами, навряд чи можна вважати успішним. Є багато показань, що програма старіння передбачає реактивні види кисню, що утворюються в мітохондрії (супероксид, перекис водню, гідроксиль радикальний). Автори спробували вимірювати надоксид у фібробластах молодих і старих людей з використанням мітосокської катації як реагенту супероксиду. Вони виявили деяке збільшення відповіді на це реагент з віком (97-річному віці 67% більше відповідь, ніж ембріон). Тим не менш, мітосок вимірює два взаємопов'язані параметри одночасно: супероксид і мітохондріальний мембранний потенціал.
Незважаючи на свою оригінальність, робота під час обговорення повинна бути попередньою. Крім того, великий розсіювання даних Гайаші та його колег не дозволяють зробити остаточний висновок про рівень перекису. І тут ми повинні, на жаль, держава, яка, незважаючи на свою оригінальність, повинна бути розглянута як чисто попередня. Неважливо, що молоді люди мали лише три і один ембріон, і похилого лише чотири, і один з найбільшим ефектом старіння (старий пацієнт 97-річного віку) був також тільки в скутальному, а другий три були між 80 і 86 років. Не серйозний геронтологічний журнал прийматиме статтю, де експериментальні когорти так дрібні. Не краще повторювати: завжди були тільки три. Ключовий експеримент щодо дії гліцину додають до фібробластів, як правило, проводиться тільки в 97-річному віці, що у порівнянні з єдиним ембріоном. Не варто збігатися з тим, що це важливе спостереження поміщається в Додаток, а не в головному тексті статті.
На жаль, є інші дослідники, які повинні повторювати цю потенційно цікава робота.Видання
P.S. І пам'ятайте, що просто змініть наше споживання – разом ми змінюємо світ!
Приєднуйтесь до нас на Facebook і VKontakte, і ми також в Однокласниках
Джерело: kot.sh/statya/233/nasha-smert-zaprogrammirovana
Як не пропустити альбоми улюблених музикантів
Він не замислювався про те, що вперше він кинув фен на банан. Вражає світ!