942
Baterías de iones de litio cumplió 25 años
Este año cumplió 25 años desde el estreno de la venta de las primeras baterías de li-ion, que ha fabricado Sony en 1991. Por un cuarto de siglo, su capacidad casi se ha duplicado desde 110 wh/kg a 200 wh/kg, pero, a pesar de este enorme progreso y en numerosos estudios electroquímicos de los mecanismos que hoy en día los procesos químicos y de materiales en el interior de baterías de li-ion prácticamente la misma que hace 25 años. En este artículo se explica cómo iba la formación y el desarrollo de esta tecnología, así como las dificultades que enfrentan hoy en día los desarrolladores de nuevos materiales.

1. El desarrollo de la tecnología: 1980-2000
Aún en 70 años los científicos se determinó que existen materiales bajo el nombre de халькогениды (por ejemplo, MoS2), que son capaces de entrar en обратимую de reaccionar con iones de litio, al incorporar en su una estructura cristalina. Inmediatamente se propuso el primer prototipo de batería de litio-ion, que consta de халькогенидов en el cátodo y el metal de litio en el ánodo. En teoría, en el momento de la descarga, los iones de litio, "liberadas" el ánodo, deben integrarse en una estructura MoS2, y durante la carga de asentarse de nuevo en el ánodo, volviendo a su estado original.
Pero los primeros intentos de creación de estas baterías no tuvieron éxito, como el caso de la carga de batería de iones de litio no querían volver a convertirse en la lisa de la placa de metal de litio, y se asentaban en el ánodo como sea, con el consiguiente aumento de las dendritas de las (cadenas de metal litio), cortocircuito, y la explosión de la batería. A esto siguió una etapa de un estudio detallado de la reacción de интеркаляции (inserción de litio en los cristales con el especial de la estructura), lo que permitió la sustitución de metal litio en carbono: en primer lugar el coque, y luego en el grafito, que se utiliza hasta ahora, y también tiene una estructura capaz de incorporar iones de litio.
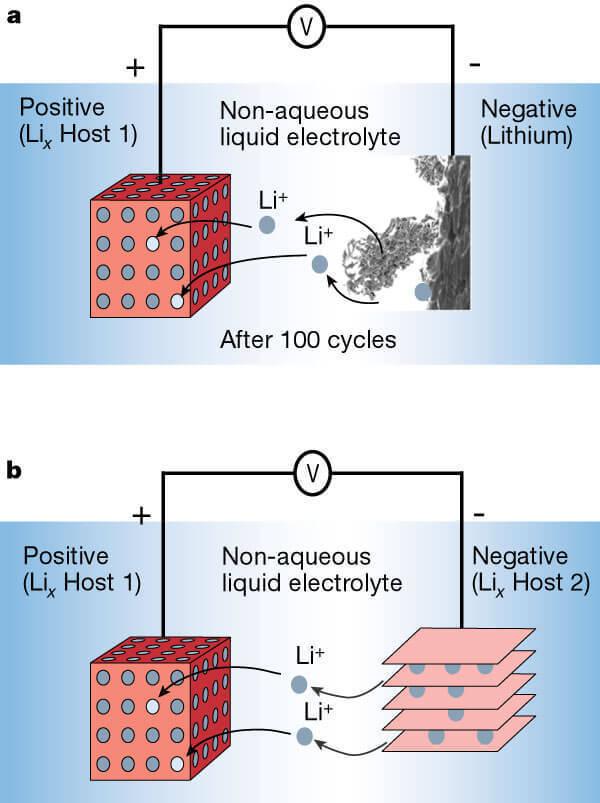
Batería de litio-ion con el ánodo de metal litio (a) y el ánodo de laminado (b).
Al comenzar a utilizar los materiales de carbón en el ánodo, los científicos se dieron cuenta de que la naturaleza hizo a la humanidad un gran regalo. En el grafito, cuando la primera carga, se forma una capa protectora de la destruida electrolito, llamado SEI (tipo Ii Interface). El mecanismo exacto de su formación y composición aún estudiado, pero se sabe que sin este singular пассивирующего de la capa de electrolito seguiría descomponerse en el ánodo electrodo habría fue destruida, y la batería llegaba en mal estado. Así surgió la primera trabaja ánodo de carbono de los materiales, que fue lanzado a la venta en la composición de baterías de li-ion en la década de los 90.
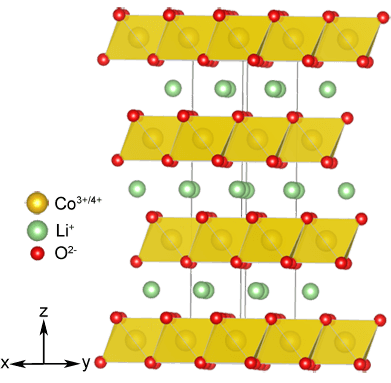
Al mismo tiempo, con el ánodo se variaba y el cátodo: se ha aclarado que la revoque, capaz de incorporar iones de litio, no sólo tienen халькогениды, pero también algunos óxidos de metales de transición, por ejemplo LiMO2 ( M = Ni, Co, Mn), que no sólo son más estables químicamente, sino que permiten crear una celda con un voltaje más alto. Y es LiCoO2 se ha utilizado en el cátodo el primer comercial de un prototipo de batería.
2. Nuevas reacciones y de la moda en nanomateriales: 2000-2010
En 2000х en la ciencia comenzó el boom de los nanomateriales. Naturalmente, los avances en la nanotecnología no ha pasado por alto y las baterías de litio. Y es gracias a ellos, los científicos hicieron perfectamente, aparentemente, no aplicable para esta tecnología, material, LiFePO4, uno de los líderes en el uso de la катодах электромобильных de las baterías.
Y la cosa es que las convencionales, las partículas железофосфата muy mal pasan los iones de sí y electrónica de la conductividad de ellos es muy baja. Pero al наноструктурирования litio no es necesario avanzar en la ampliación de la distancia para encajar en la нанокристалл, por lo tanto, интеркаляция pasa mucho más rápido, mientras que el revestimiento de нанокристаллов fina de carbono de la película mejora la conductividad. En consecuencia, la venta ha salido a no menos de un material peligroso, que no distingue el oxígeno a alta temperatura (óxidos), sino que el material tiene la capacidad de trabajar en más de corrientes altas. Es por ello que катодный material prefieren los fabricantes de coches, a pesar de un poco menor capacidad que el de LiCoO2.
Al mismo tiempo, los científicos en busca de nuevos materiales que interactúan con el litio. Y, como se ha aclarado, интеркаляция, o la inserción de litio en el cristal no es la única variante de la reacción en los electrodos en baterías de iones de litio de la batería. Así, por ejemplo, algunos elementos, a saber, Si, Sn, Sb, etc., forman una "aleación" con el litio, si se utilizan en el ánodo. La capacidad de este electrodo 10 veces superior a la capacidad de grafito, pero hay un "pero": un electrodo en el momento de la formación de la aleación fuerte aumento de volumen, lo que conduce a una rápida formación de grietas y la llegada a la inutilidad. Y para reducir la tensión del electrodo para el mismo aumento de volumen, el elemento (por ejemplo, el silicio) permitir usar en forma de nanopartículas, de los presos en la matriz de carbón, que "protegen" los cambios de volumen.

Pero los cambios de volumen no es el único problema de los materiales que forman las aleaciones de aluminio, y que obstaculiza su amplia aplicación. Como se mencionó anteriormente, en el grafito se forma "un regalo de la naturaleza"- SEI. Y en los materiales que forman la aleación, el electrolito se descompone de forma continua y aumenta la resistencia del electrodo. Pero sin embargo, periódicamente, nos vemos en las noticias, que en algunos batería se utiliza el "ánodo de silicio". Sí, el silicio es verdad que se utiliza, pero en cantidades muy pequeñas y mezclado con grafito para "efectos secundarios" no demasiado visibles. Naturalmente, cuando la cantidad de silicio en el ánodo es de sólo unos pocos por ciento, y el resto - el grafito, el aumento significativo de la capacidad no va a funcionar.
Y si el tema de los ánodos, forman aleaciones, ahora se desarrolla, algunos estudios iniciados en la década pasada, muy rápidamente metimos en un callejón sin salida. Es el caso, por ejemplo, de los llamados de las reacciones de conversión. En esta reacción de algunos compuestos de metales (óxidos, nitruros, sulfuros, etc.) interactúan con el litio, que se convierte en el metal, mezclado con conexiones de litio:
MaXb ==> aM + bLinX
M: metal
X: O, N, C, S...
Y, como se puede imaginar, con el material en el momento de la reacción se producen tales cambios, que incluso кремнию no soñaban. Por ejemplo, el óxido de cobalto se convierte en nanopartículas de metal de cobalto, presos en una matriz de óxido de litio:
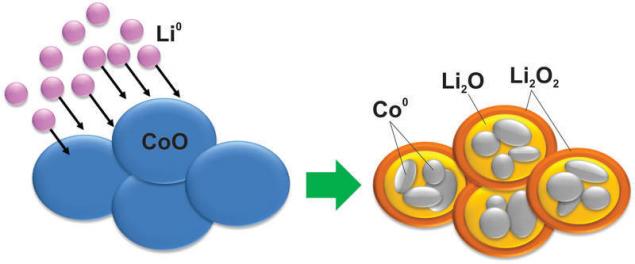
Naturalmente, esta reacción malo es reversible, de la misma entre la carga y la descarga de la gran diferencia de voltaje que hace que estos materiales inútiles en la aplicación.
Es interesante notar que cuando esta reacción fue descubierta en revistas científicas se han publicado cientos de artículos sobre este tema. Pero aquí хочестся citar profesor de Tarascon de la Universidad de france, quien dijo que "la reacción de la tasa de conversión se presente un campo de experimentación para el estudio de materiales con наноархитектурой, que dio a los científicos la oportunidad de hacer buenas fotos con el que trasluce del microscopio electrónico y se publicarán en conocidas revistas, a pesar de la absoluta práctico de la inutilidad de estos materiales".
En general, si resumir, entonces, a pesar de que en la última década, se han sintetizado cientos de nuevos materiales para electrodos de la batería hasta ahora bajo se utilizan prácticamente los mismos materiales, que hace 25 años. ¿Por qué sucedió?
3. Actualidad: las dificultades en el desarrollo de nuevas baterías.
Como se puede observar en la anterior digresión lejana histórica en la historia de baterías de li-ion ni una palabra no se ha dicho sobre el otro, el más importante elemento: el electrolito. Y con razón: el electrolito de 25 años, prácticamente no ha cambiado y trabajan alternativas sugirió que no era. Hoy, como en la década de los 90, en la forma de un electrolito se utilizan sales de litio (principalmente LiPF6) en la disolución de los carbonatos (carbonato de etileno (EC) + dimetil carbonato (DMC)). Y es precisamente debido a la electrolito progreso en el aumento de la capacidad de la batería en los últimos años se ha ralentizado.
Daré un ejemplo concreto: hoy en día existen materiales para los electrodos, que podrían aumentar considerablemente la capacidad de la batería li-ion de la batería. A ellos se refiere, por ejemplo, LiNi0.5Mn1.5О4, que permita hacer de la batería con una tensión de celda en 5 Voltios. Pero por desgracia, en las bandas de tensión de un electrolito a base de carbonatos se vuelve inestable. O otro ejemplo: como se mencionó anteriormente, hoy en día, para utilizar importantes cantidades de silicio (o de otros metales, formando aleaciones con el litio en el ánodo, es necesario resolver uno de los principales problemas de la educación пассивирующего de la capa (SEI), que dejó a la continua descomposición del electrolito y la destrucción del electrodo, y para ello tenemos que inventar un nuevo composición del electrolito. Pero, ¿por qué es tan difícil encontrar una alternativa existente a la composición, ya que las sales de litio completamente, sí y solventes orgánicos es suficiente?!
Y la dificultad de заключаетя en el hecho de que el electrolito debe tener las siguientes características:
En paralelo con la mejora de las tecnologías existentes, los científicos trabajamos fundamentalmente con nuevas soluciones. Y la decisión de estos se puede reducir a un intento de deshacerse de líquido disolvente a base de carbonatos. A esas tecnologías se refieren, por ejemplo, iones de líquido. Iones del líquido es, en realidad, fundidos de la sal, que es muy baja temperatura de fusión, y algunos de ellos incluso a temperatura ambiente permanecen líquidos. Y todo por el hecho de que estas sales especial, стерически затрудненная estructura que complicarn la cristalización.
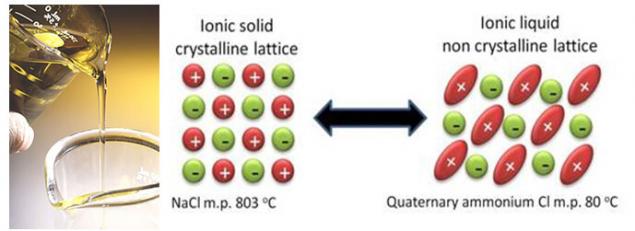
Aparentemente, la idea de excluir por completo el disolvente, que es inflamable y entrará en parásitos de la reacción con el litio. Pero en realidad, la exclusión de disolventes crea en el momento más problemas de los que resuelve. En primer lugar, en las electroquímica parte del disolvente "sacrifica" para crear una capa protectora en la superficie de los electrodos. Y los componentes de iones líquidos con esta tarea hasta que no lo hacen (aniones, por cierto, también pueden contraer parásitos de la reacción de los electrodos, como disolventes). En segundo lugar, es muy difícil de recoger el líquido iónico con la correcta anión, ya que no sólo afectan a la temperatura de fusión de la sal, pero en electroquímica, la estabilidad. Y por desgracia, las más estables aniones forman la sal, que se funden a temperaturas más elevadas y, en consecuencia, al contrario.
Otra manera de deshacerse de solvente a base de carbonatos - uso de polímeros (por ejemplo, poliésteres), conductoras de litio, que, en primer lugar, minimicen el riesgo de fuga hacia el exterior, sino también interfieren en el crecimiento de las dendritas de las cuando se utiliza un metal de litio en el ánodo. Pero la principal dificultad que enfrentan los creadores de electrolitos poliméricos - muy baja conductividad iónica, así como iones de litio es difícil moverse en un viscoso entorno. Esto, por supuesto, limita la potencia de la batería. Y reducir la viscosidad conlleva la germinación de las dendritas de las.

Además, los investigadores estudian los sólidos inorgánicos, sustancias conductoras de litio con defectos en el cristal, y tratando de aplicar en forma de electrolitos para baterías de li-ion. Este sistema a primera vista ideal: la química y electroquímica de la estabilidad, la resistencia con la temperatura y la resistencia mecánica. Pero junto a estos materiales, una vez más, la muy baja conductividad iónica, y el uso de sus целесеобразно sólo en la forma de películas delgadas. Además, trabajan materiales como el mejor de la alta temperatura. Y la última, con un electrolito es muy difícil crear un contacto mecánico entre электолитом y los electrodos (en esta esfera líquida de электролитам no igual).
4. Conclusión.
Desde el momento de la salida a la venta de baterías de ión litio, el intento de aumentar su capacidad de no cesan. Pero en los últimos años, el aumento de la capacidad se ha desacelerado, a pesar de cientos de nuevas propuestas de materiales para los electrodos. Y la cosa es que la mayoría de estos nuevos materiales "están en la estantería" y espera hasta que aparezca la nueva, ideal para sus necesidades de electrolitos. Y el desarrollo de nuevos electrolitos - en mi opinión es mucho más complicado que el desarrollo de nuevos electrodos, así como tomar en cuenta no sólo las propiedades electroquímicas del electrolito, pero todas sus interacciones con los electrodos. En general, la lectura de noticias tipo ", ha sido desarrollado un nuevo super-electrodo..." es necesario comprobar que, como tal, el electrodo se comunica con el electrolito, y si hay para este tipo de electrodo adecuado de electrolitos en principio. publicado
Fuente: geektimes.ru/post/282424/

1. El desarrollo de la tecnología: 1980-2000
Aún en 70 años los científicos se determinó que existen materiales bajo el nombre de халькогениды (por ejemplo, MoS2), que son capaces de entrar en обратимую de reaccionar con iones de litio, al incorporar en su una estructura cristalina. Inmediatamente se propuso el primer prototipo de batería de litio-ion, que consta de халькогенидов en el cátodo y el metal de litio en el ánodo. En teoría, en el momento de la descarga, los iones de litio, "liberadas" el ánodo, deben integrarse en una estructura MoS2, y durante la carga de asentarse de nuevo en el ánodo, volviendo a su estado original.
Pero los primeros intentos de creación de estas baterías no tuvieron éxito, como el caso de la carga de batería de iones de litio no querían volver a convertirse en la lisa de la placa de metal de litio, y se asentaban en el ánodo como sea, con el consiguiente aumento de las dendritas de las (cadenas de metal litio), cortocircuito, y la explosión de la batería. A esto siguió una etapa de un estudio detallado de la reacción de интеркаляции (inserción de litio en los cristales con el especial de la estructura), lo que permitió la sustitución de metal litio en carbono: en primer lugar el coque, y luego en el grafito, que se utiliza hasta ahora, y también tiene una estructura capaz de incorporar iones de litio.

Batería de litio-ion con el ánodo de metal litio (a) y el ánodo de laminado (b).
Al comenzar a utilizar los materiales de carbón en el ánodo, los científicos se dieron cuenta de que la naturaleza hizo a la humanidad un gran regalo. En el grafito, cuando la primera carga, se forma una capa protectora de la destruida electrolito, llamado SEI (tipo Ii Interface). El mecanismo exacto de su formación y composición aún estudiado, pero se sabe que sin este singular пассивирующего de la capa de electrolito seguiría descomponerse en el ánodo electrodo habría fue destruida, y la batería llegaba en mal estado. Así surgió la primera trabaja ánodo de carbono de los materiales, que fue lanzado a la venta en la composición de baterías de li-ion en la década de los 90.
Al mismo tiempo, con el ánodo se variaba y el cátodo: se ha aclarado que la revoque, capaz de incorporar iones de litio, no sólo tienen халькогениды, pero también algunos óxidos de metales de transición, por ejemplo LiMO2 ( M = Ni, Co, Mn), que no sólo son más estables químicamente, sino que permiten crear una celda con un voltaje más alto. Y es LiCoO2 se ha utilizado en el cátodo el primer comercial de un prototipo de batería.

2. Nuevas reacciones y de la moda en nanomateriales: 2000-2010
En 2000х en la ciencia comenzó el boom de los nanomateriales. Naturalmente, los avances en la nanotecnología no ha pasado por alto y las baterías de litio. Y es gracias a ellos, los científicos hicieron perfectamente, aparentemente, no aplicable para esta tecnología, material, LiFePO4, uno de los líderes en el uso de la катодах электромобильных de las baterías.
Y la cosa es que las convencionales, las partículas железофосфата muy mal pasan los iones de sí y electrónica de la conductividad de ellos es muy baja. Pero al наноструктурирования litio no es necesario avanzar en la ampliación de la distancia para encajar en la нанокристалл, por lo tanto, интеркаляция pasa mucho más rápido, mientras que el revestimiento de нанокристаллов fina de carbono de la película mejora la conductividad. En consecuencia, la venta ha salido a no menos de un material peligroso, que no distingue el oxígeno a alta temperatura (óxidos), sino que el material tiene la capacidad de trabajar en más de corrientes altas. Es por ello que катодный material prefieren los fabricantes de coches, a pesar de un poco menor capacidad que el de LiCoO2.
Al mismo tiempo, los científicos en busca de nuevos materiales que interactúan con el litio. Y, como se ha aclarado, интеркаляция, o la inserción de litio en el cristal no es la única variante de la reacción en los electrodos en baterías de iones de litio de la batería. Así, por ejemplo, algunos elementos, a saber, Si, Sn, Sb, etc., forman una "aleación" con el litio, si se utilizan en el ánodo. La capacidad de este electrodo 10 veces superior a la capacidad de grafito, pero hay un "pero": un electrodo en el momento de la formación de la aleación fuerte aumento de volumen, lo que conduce a una rápida formación de grietas y la llegada a la inutilidad. Y para reducir la tensión del electrodo para el mismo aumento de volumen, el elemento (por ejemplo, el silicio) permitir usar en forma de nanopartículas, de los presos en la matriz de carbón, que "protegen" los cambios de volumen.

Pero los cambios de volumen no es el único problema de los materiales que forman las aleaciones de aluminio, y que obstaculiza su amplia aplicación. Como se mencionó anteriormente, en el grafito se forma "un regalo de la naturaleza"- SEI. Y en los materiales que forman la aleación, el electrolito se descompone de forma continua y aumenta la resistencia del electrodo. Pero sin embargo, periódicamente, nos vemos en las noticias, que en algunos batería se utiliza el "ánodo de silicio". Sí, el silicio es verdad que se utiliza, pero en cantidades muy pequeñas y mezclado con grafito para "efectos secundarios" no demasiado visibles. Naturalmente, cuando la cantidad de silicio en el ánodo es de sólo unos pocos por ciento, y el resto - el grafito, el aumento significativo de la capacidad no va a funcionar.
Y si el tema de los ánodos, forman aleaciones, ahora se desarrolla, algunos estudios iniciados en la década pasada, muy rápidamente metimos en un callejón sin salida. Es el caso, por ejemplo, de los llamados de las reacciones de conversión. En esta reacción de algunos compuestos de metales (óxidos, nitruros, sulfuros, etc.) interactúan con el litio, que se convierte en el metal, mezclado con conexiones de litio:
MaXb ==> aM + bLinX
M: metal
X: O, N, C, S...
Y, como se puede imaginar, con el material en el momento de la reacción se producen tales cambios, que incluso кремнию no soñaban. Por ejemplo, el óxido de cobalto se convierte en nanopartículas de metal de cobalto, presos en una matriz de óxido de litio:

Naturalmente, esta reacción malo es reversible, de la misma entre la carga y la descarga de la gran diferencia de voltaje que hace que estos materiales inútiles en la aplicación.
Es interesante notar que cuando esta reacción fue descubierta en revistas científicas se han publicado cientos de artículos sobre este tema. Pero aquí хочестся citar profesor de Tarascon de la Universidad de france, quien dijo que "la reacción de la tasa de conversión se presente un campo de experimentación para el estudio de materiales con наноархитектурой, que dio a los científicos la oportunidad de hacer buenas fotos con el que trasluce del microscopio electrónico y se publicarán en conocidas revistas, a pesar de la absoluta práctico de la inutilidad de estos materiales".
En general, si resumir, entonces, a pesar de que en la última década, se han sintetizado cientos de nuevos materiales para electrodos de la batería hasta ahora bajo se utilizan prácticamente los mismos materiales, que hace 25 años. ¿Por qué sucedió?
3. Actualidad: las dificultades en el desarrollo de nuevas baterías.
Como se puede observar en la anterior digresión lejana histórica en la historia de baterías de li-ion ni una palabra no se ha dicho sobre el otro, el más importante elemento: el electrolito. Y con razón: el electrolito de 25 años, prácticamente no ha cambiado y trabajan alternativas sugirió que no era. Hoy, como en la década de los 90, en la forma de un electrolito se utilizan sales de litio (principalmente LiPF6) en la disolución de los carbonatos (carbonato de etileno (EC) + dimetil carbonato (DMC)). Y es precisamente debido a la electrolito progreso en el aumento de la capacidad de la batería en los últimos años se ha ralentizado.
Daré un ejemplo concreto: hoy en día existen materiales para los electrodos, que podrían aumentar considerablemente la capacidad de la batería li-ion de la batería. A ellos se refiere, por ejemplo, LiNi0.5Mn1.5О4, que permita hacer de la batería con una tensión de celda en 5 Voltios. Pero por desgracia, en las bandas de tensión de un electrolito a base de carbonatos se vuelve inestable. O otro ejemplo: como se mencionó anteriormente, hoy en día, para utilizar importantes cantidades de silicio (o de otros metales, formando aleaciones con el litio en el ánodo, es necesario resolver uno de los principales problemas de la educación пассивирующего de la capa (SEI), que dejó a la continua descomposición del electrolito y la destrucción del electrodo, y para ello tenemos que inventar un nuevo composición del electrolito. Pero, ¿por qué es tan difícil encontrar una alternativa existente a la composición, ya que las sales de litio completamente, sí y solventes orgánicos es suficiente?!
Y la dificultad de заключаетя en el hecho de que el electrolito debe tener las siguientes características:
- Él debe ser químicamente estable durante el tiempo de funcionamiento de la batería, sino más bien, debe ser persistente con respecto a окисляющему el cátodo y disfrutar de una pausa el ánodo. Esto significa que los intentos de aumentar la intensidad de la energía de la batería, es decir, el uso más oxidantes cátodos y recuperación de los ánodos, no deben dar lugar a la descomposición del electrolito.
- El electrolito también debe tener una buena conductividad iónica y de baja viscosidad para el transporte de los iones de litio en un amplio rango de temperaturas. Para ello, en viscosa carbonato de etileno añaden DMC a partir de 1994.
- Sal de litio deben disolverse en un solvente orgánico.
- El electrolito debe establecer un eficaz пассивирующий capa. El carbonato de etileno es un bien se obtiene, mientras que otros disolventes, por ejemplo, carbonato de propileno, que ha sido probado por Sony, destruye la estructura del ánodo, ya que se integra en él, en paralelo con el litio.
En paralelo con la mejora de las tecnologías existentes, los científicos trabajamos fundamentalmente con nuevas soluciones. Y la decisión de estos se puede reducir a un intento de deshacerse de líquido disolvente a base de carbonatos. A esas tecnologías se refieren, por ejemplo, iones de líquido. Iones del líquido es, en realidad, fundidos de la sal, que es muy baja temperatura de fusión, y algunos de ellos incluso a temperatura ambiente permanecen líquidos. Y todo por el hecho de que estas sales especial, стерически затрудненная estructura que complicarn la cristalización.

Aparentemente, la idea de excluir por completo el disolvente, que es inflamable y entrará en parásitos de la reacción con el litio. Pero en realidad, la exclusión de disolventes crea en el momento más problemas de los que resuelve. En primer lugar, en las electroquímica parte del disolvente "sacrifica" para crear una capa protectora en la superficie de los electrodos. Y los componentes de iones líquidos con esta tarea hasta que no lo hacen (aniones, por cierto, también pueden contraer parásitos de la reacción de los electrodos, como disolventes). En segundo lugar, es muy difícil de recoger el líquido iónico con la correcta anión, ya que no sólo afectan a la temperatura de fusión de la sal, pero en electroquímica, la estabilidad. Y por desgracia, las más estables aniones forman la sal, que se funden a temperaturas más elevadas y, en consecuencia, al contrario.
Otra manera de deshacerse de solvente a base de carbonatos - uso de polímeros (por ejemplo, poliésteres), conductoras de litio, que, en primer lugar, minimicen el riesgo de fuga hacia el exterior, sino también interfieren en el crecimiento de las dendritas de las cuando se utiliza un metal de litio en el ánodo. Pero la principal dificultad que enfrentan los creadores de electrolitos poliméricos - muy baja conductividad iónica, así como iones de litio es difícil moverse en un viscoso entorno. Esto, por supuesto, limita la potencia de la batería. Y reducir la viscosidad conlleva la germinación de las dendritas de las.

Además, los investigadores estudian los sólidos inorgánicos, sustancias conductoras de litio con defectos en el cristal, y tratando de aplicar en forma de electrolitos para baterías de li-ion. Este sistema a primera vista ideal: la química y electroquímica de la estabilidad, la resistencia con la temperatura y la resistencia mecánica. Pero junto a estos materiales, una vez más, la muy baja conductividad iónica, y el uso de sus целесеобразно sólo en la forma de películas delgadas. Además, trabajan materiales como el mejor de la alta temperatura. Y la última, con un electrolito es muy difícil crear un contacto mecánico entre электолитом y los electrodos (en esta esfera líquida de электролитам no igual).
4. Conclusión.
Desde el momento de la salida a la venta de baterías de ión litio, el intento de aumentar su capacidad de no cesan. Pero en los últimos años, el aumento de la capacidad se ha desacelerado, a pesar de cientos de nuevas propuestas de materiales para los electrodos. Y la cosa es que la mayoría de estos nuevos materiales "están en la estantería" y espera hasta que aparezca la nueva, ideal para sus necesidades de electrolitos. Y el desarrollo de nuevos electrolitos - en mi opinión es mucho más complicado que el desarrollo de nuevos electrodos, así como tomar en cuenta no sólo las propiedades electroquímicas del electrolito, pero todas sus interacciones con los electrodos. En general, la lectura de noticias tipo ", ha sido desarrollado un nuevo super-electrodo..." es necesario comprobar que, como tal, el electrodo se comunica con el electrolito, y si hay para este tipo de electrodo adecuado de electrolitos en principio. publicado
Fuente: geektimes.ru/post/282424/
Las pilas pueden convertir desechos en energía limpia
SolarStratos: el avión solar, que se eleva a la estratosfera