488
Моделювання фотосинтезу
Коли ви думаєте про геній природи (неважливо, що кладе будь-яке значення в слово Nature), я хочу сказати, що її корона людство, індивіди, з яких, гордо розміщуючи ноутбук на животі, роблять те, що протягом декількох десятиліть ви можете тільки мріяти про: спілкуватися з усього світу!
Але з екологічної точки зору наш вид є тільки споживачем одного з найвищих замовлень, що відпочивають на лаврах тих, хто створює біомасу від інанімату, тобто на лаврах наших братів автотрофічних рослин.
Зауважте, що велика більшість рослин не просто автотрофи, а фотоаутотрофи, тобто для синтезу органічних сполук з неорганічних використовують енергію фотонів, джерело яких є Сонце. Не дивно, що спроби не тільки відтворити процес фотосинтезу, але перехопити його і покласти її на широку ногу отримувати стільки уваги від вчених.
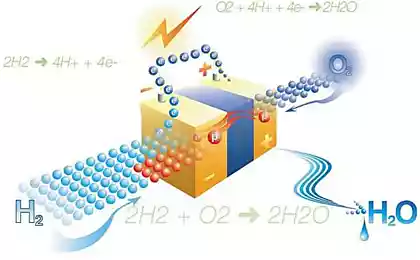
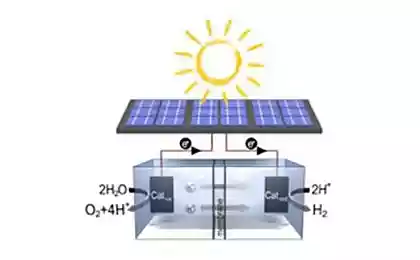
Як відомо, побічний продукт фотосинтезу є киснем, що виробляється окисленням води під дією фотосистеми II (FS II). Нагадуйте, як це працює.
квантовий світлих хітів хлорофіла, вибиває електрону з неї. Цей електрон потім в кінцевому підсумку входить до фотосистеми I, і позбавив його хлорофілу, який став сильним окислювачем, бере електрони з води через марганець-контейнерний комплекс окислення води (VOC), в результаті чого утворюється кисень.
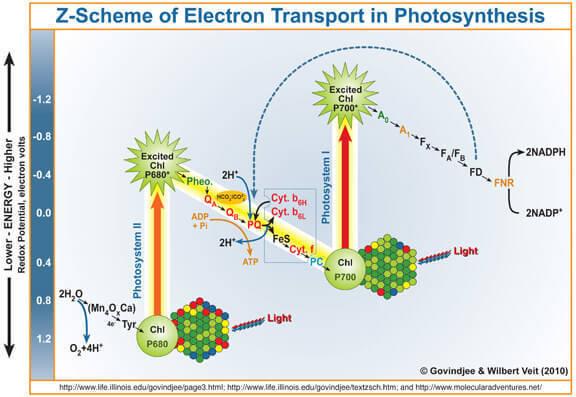
Таким чином, OOC може розглядатися як каталізатор для процесу окислення води. Це імітація цієї частини FS II, які дослідники активно займаються.
Я повинен сказати, що потенційно (тобто термодинамічно) вода може окиснути будь-який окислювач, потенціал електрода якого вище його електродного потенціалу. Наприклад, марганат калію (E°=+1.51 В за півреакцію MnO4+5e+8H+ → Mn2+++4H2O). Ви можете подивитися на таблицю стандартних електродних потенціалів і переконатися, що є інші приклади. Тим не менш, на практиці це не буває для кінетичних причин, іншими словами, через високу енергію активації, швидкість цього процесу дуже невелика. Саме тому розвиток каталізатора для окислення води актуальний, а біоміметичний підхід перспективний.
У однорідному каталізі (тобто в каталітичної реакції, в якій каталізатор знаходиться в тій же фазі, як реагенти, на практиці - в основному в рідині), активність каталізатора зазвичай оцінюється таким параметром, як "швидкість обертання" (TOF, частота обороту), тобто кількість молекул реагенту, перетворених однією молекулою каталізатора (точніше - активний центр) в одиницю часу, має вимір c-1. GOC FS II має TOF близько 100-400 s-1.
Дослідники з університету Вюрцбург вирішили використовувати ірентійський комплекс, що містить 3 атоми цього елемента [Ru(bda)bpb]3 як каталізатор для водовідведення.
«Чому рутенію?» запитати, і я відповість: очевидно, тому що набір окислювальних ступенів цього елемента (+2, +3, +4, +5) боляче нагадує набір ступенів окислення марганцю, які, як вважають дослідники, приймають його атоми в СО при окисленні води.
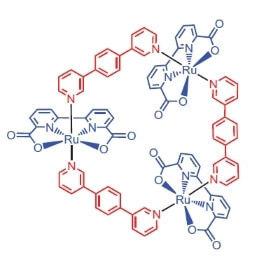
Що робить це ганчінка?
У водяно-ацетонітриловій суміші на pH=1, вона здатна каталізувати окислення води з амоніумом-цетрієм (IV) нітратом (E°=+1.72 V для Ce4++e- → Ce3+ half-reaction). Як тільки цей сильний окислювач додається в систему, що містить невелику кількість каталізаторів, кисневі бульбашки відразу починають випускатися, концентрація якого в газовій фазі над розчином різко підвищується! TOF цього каталізатора близько до ефективності природного WOC і становить близько 160 с-1. Реакція 2Ce4 + H2O → 2Ce3 + 1/2O2 + 2H+.
2433699
Проте вчені не зупинилися. Дослідники вирішили розробити систему, яка буде працювати фотохімічно, тобто, в якомусь чином, мігмітувати роботу FS II. Другий ключовий програвач в цьому біоміметичного дизайну був ще одним ірентійським комплексом як фотосенсибілізатор. Ось як працює.
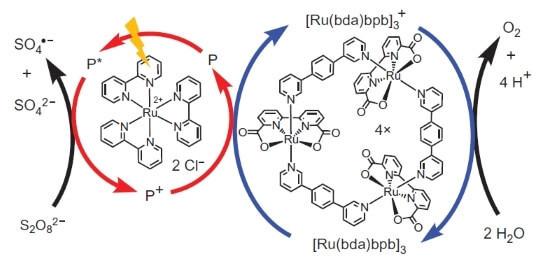
Фотон (душ як блискавка) вибиває електрон з фотосенсибілізатора (коло червоних стрілок). Електрон «злівий хід», до зовнішнього приймальника, пероксодисульфурат натрію (E°=+2.01 В для напівреакції S2O82-+2e- → 2SO42-), а отвір, яке в нашому випадку представлена атомом іржі з окисленням (+3), окислює каталізатор (окіль сильних стріл), який в свою чергу займає електрону з води. Таким чином, загальний рівень реакції S2O82-+H2O → 2SO42-+1/2O2+2H+.
Яка перевага каталізатора, створеного німецькими дослідниками?
1) Входить в дуже невелику і елітну групу каталізаторів, здатних досягати TOF в надлишку 100 s-1. На фотохімічному процесі випуск кисню вже помітний при концентрації каталізатора близько 90 нМ, тобто 90×10-9 mol / л.
2) У зв'язку з тим, що каталізично активні атоми рутенію міцно підключені, як літати в Інтернеті, полідентними лігандами, комплексний каталізатор більш стійкий, ніж його мононуклеючі аналоги.
Стійкість каталізатора характеризується таким параметром, як «номер революцій» (ТОН, число оборотів) - кількість каталітичних циклів, які активний центр може перетворюватися до моменту деактивації (застосування). У реакції окислення води під дією Ce(IV), TON становить близько 7400 для неї проти 1000 мононуклейних аналогів. Однак в разі фотохімічного процесу ТОН нижче (резистентність менше) - близько 1200.
І недоліки.
У статті про відкриття нового каталізатора опублікована в журналі Nature (Nature Chemistry), яка публікує найбільш прогресивну і найважливішу роботу для хімічної спільноти і, ймовірно, для людства (імпакт-фактор 2014 – 25.3).
Проксимус Все, що людство може зробити сьогодні за допомогою не найдешевших металевих ірентій (чеп марганець працює в природі) в 0.1 n сірчаної кислоти (pH = 1, про цю кислотність, трохи нижче, в шлунку; окислення води в природі відбувається на pH близько 7) і 60% ацетонітрил (органічний розчинник, який не потрібно хлоропластами) дають десятки мікромолів кисню на другий. Але є те, що ви прагнете! Видання
P.S. І пам'ятайте, що просто змініть наше споживання – разом ми змінюємо світ!
Приєднуйтесь до нас на Facebook, VKontakte, Odnoklassniki
Джерело: geektimes.ru/post/275460/
Але з екологічної точки зору наш вид є тільки споживачем одного з найвищих замовлень, що відпочивають на лаврах тих, хто створює біомасу від інанімату, тобто на лаврах наших братів автотрофічних рослин.
Зауважте, що велика більшість рослин не просто автотрофи, а фотоаутотрофи, тобто для синтезу органічних сполук з неорганічних використовують енергію фотонів, джерело яких є Сонце. Не дивно, що спроби не тільки відтворити процес фотосинтезу, але перехопити його і покласти її на широку ногу отримувати стільки уваги від вчених.
Як відомо, побічний продукт фотосинтезу є киснем, що виробляється окисленням води під дією фотосистеми II (FS II). Нагадуйте, як це працює.
квантовий світлих хітів хлорофіла, вибиває електрону з неї. Цей електрон потім в кінцевому підсумку входить до фотосистеми I, і позбавив його хлорофілу, який став сильним окислювачем, бере електрони з води через марганець-контейнерний комплекс окислення води (VOC), в результаті чого утворюється кисень.

Таким чином, OOC може розглядатися як каталізатор для процесу окислення води. Це імітація цієї частини FS II, які дослідники активно займаються.
Я повинен сказати, що потенційно (тобто термодинамічно) вода може окиснути будь-який окислювач, потенціал електрода якого вище його електродного потенціалу. Наприклад, марганат калію (E°=+1.51 В за півреакцію MnO4+5e+8H+ → Mn2+++4H2O). Ви можете подивитися на таблицю стандартних електродних потенціалів і переконатися, що є інші приклади. Тим не менш, на практиці це не буває для кінетичних причин, іншими словами, через високу енергію активації, швидкість цього процесу дуже невелика. Саме тому розвиток каталізатора для окислення води актуальний, а біоміметичний підхід перспективний.
У однорідному каталізі (тобто в каталітичної реакції, в якій каталізатор знаходиться в тій же фазі, як реагенти, на практиці - в основному в рідині), активність каталізатора зазвичай оцінюється таким параметром, як "швидкість обертання" (TOF, частота обороту), тобто кількість молекул реагенту, перетворених однією молекулою каталізатора (точніше - активний центр) в одиницю часу, має вимір c-1. GOC FS II має TOF близько 100-400 s-1.
Дослідники з університету Вюрцбург вирішили використовувати ірентійський комплекс, що містить 3 атоми цього елемента [Ru(bda)bpb]3 як каталізатор для водовідведення.
«Чому рутенію?» запитати, і я відповість: очевидно, тому що набір окислювальних ступенів цього елемента (+2, +3, +4, +5) боляче нагадує набір ступенів окислення марганцю, які, як вважають дослідники, приймають його атоми в СО при окисленні води.

Що робить це ганчінка?
У водяно-ацетонітриловій суміші на pH=1, вона здатна каталізувати окислення води з амоніумом-цетрієм (IV) нітратом (E°=+1.72 V для Ce4++e- → Ce3+ half-reaction). Як тільки цей сильний окислювач додається в систему, що містить невелику кількість каталізаторів, кисневі бульбашки відразу починають випускатися, концентрація якого в газовій фазі над розчином різко підвищується! TOF цього каталізатора близько до ефективності природного WOC і становить близько 160 с-1. Реакція 2Ce4 + H2O → 2Ce3 + 1/2O2 + 2H+.
2433699
Проте вчені не зупинилися. Дослідники вирішили розробити систему, яка буде працювати фотохімічно, тобто, в якомусь чином, мігмітувати роботу FS II. Другий ключовий програвач в цьому біоміметичного дизайну був ще одним ірентійським комплексом як фотосенсибілізатор. Ось як працює.

Фотон (душ як блискавка) вибиває електрон з фотосенсибілізатора (коло червоних стрілок). Електрон «злівий хід», до зовнішнього приймальника, пероксодисульфурат натрію (E°=+2.01 В для напівреакції S2O82-+2e- → 2SO42-), а отвір, яке в нашому випадку представлена атомом іржі з окисленням (+3), окислює каталізатор (окіль сильних стріл), який в свою чергу займає електрону з води. Таким чином, загальний рівень реакції S2O82-+H2O → 2SO42-+1/2O2+2H+.
Яка перевага каталізатора, створеного німецькими дослідниками?
1) Входить в дуже невелику і елітну групу каталізаторів, здатних досягати TOF в надлишку 100 s-1. На фотохімічному процесі випуск кисню вже помітний при концентрації каталізатора близько 90 нМ, тобто 90×10-9 mol / л.
2) У зв'язку з тим, що каталізично активні атоми рутенію міцно підключені, як літати в Інтернеті, полідентними лігандами, комплексний каталізатор більш стійкий, ніж його мононуклеючі аналоги.
Стійкість каталізатора характеризується таким параметром, як «номер революцій» (ТОН, число оборотів) - кількість каталітичних циклів, які активний центр може перетворюватися до моменту деактивації (застосування). У реакції окислення води під дією Ce(IV), TON становить близько 7400 для неї проти 1000 мононуклейних аналогів. Однак в разі фотохімічного процесу ТОН нижче (резистентність менше) - близько 1200.
І недоліки.
У статті про відкриття нового каталізатора опублікована в журналі Nature (Nature Chemistry), яка публікує найбільш прогресивну і найважливішу роботу для хімічної спільноти і, ймовірно, для людства (імпакт-фактор 2014 – 25.3).
Проксимус Все, що людство може зробити сьогодні за допомогою не найдешевших металевих ірентій (чеп марганець працює в природі) в 0.1 n сірчаної кислоти (pH = 1, про цю кислотність, трохи нижче, в шлунку; окислення води в природі відбувається на pH близько 7) і 60% ацетонітрил (органічний розчинник, який не потрібно хлоропластами) дають десятки мікромолів кисню на другий. Але є те, що ви прагнете! Видання
P.S. І пам'ятайте, що просто змініть наше споживання – разом ми змінюємо світ!
Приєднуйтесь до нас на Facebook, VKontakte, Odnoklassniki
Джерело: geektimes.ru/post/275460/