821
Stanford mejorado la electrólisis del agua forma más barata

En agosto pasado, los científicos de la Universidad de Stanford han demostrado por primera vez forma barata de la electrólisis del agua, es decir, la separación de H 2 sub> O en hidrógeno y oxígeno. Para iniciar un proceso químico baterías AAA bastante simples. Por supuesto, las baterías se pueden utilizar en lugar de un pequeño panel solar que proporciona una diferencia de potencial al menos 1, 5 voltios.
En el pasado, los científicos han utilizado los cátodos y ánodos de níquel y óxido de níquel. Esta es la primera vez en la experiencia del mundo cuando la electrólisis fue capaz de abandonar a los electrodos de metales preciosos (platino, iridio), y cuando el proceso se va a una tensión tan baja.
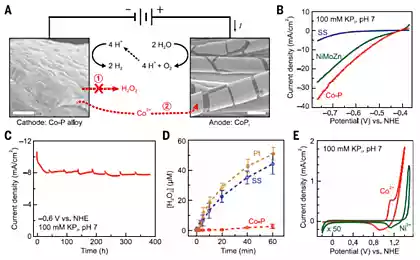
Ahora que fueron capaces de reducir el coste y simplificar más la electrólisis, lo que haría de combustible de hidrógeno más barato si la tecnología de visualización en una escala industrial. En la tecnología de proceso mejorado para el cátodo y el ánodo se utiliza el mismo catalizador de NiFeO x sub>. Es decir, el ánodo y el cátodo ya no es requerir diferente pH-factor de (uno ácida, alcalina otro) de manera que se pueden colocar fácilmente y convenientemente en un recipiente común con agua. Sólo podemos recolectar productos de oxígeno e hidrógeno (aunque es mejor no para recoger oxígeno, y de inmediato para liberar a la atmósfera).
El siguiente video muestra cómo la electrólisis de pilas AAA. Con un electrodo, oxígeno, y con otro - de hidrógeno. Autores de trabajos científicos dicen que la intensidad de la reacción es aún mayor que con la combinación del óxido de iridio tradicional electrodo y el platino.
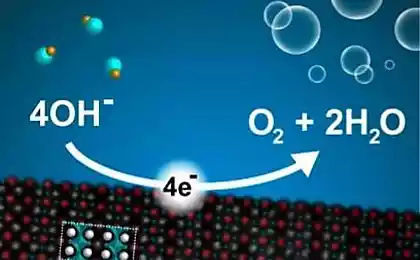
Reacción sale de manera constante y muy activo en toda la superficie de los electrodos.
El secreto del "foco" - en la estructura del catalizador NiFeO x sub>. Mientras que este aparentemente simples materiales, pero la estructura del material es muy específico. Él de alguna manera "crecido" en nanofibras de carbono (de la investigación no está claro cómo hacerlo). Los científicos dicen que esta maravillosa catalizador en el futuro puede ser adaptado para otras reacciones químicas, a excepción de la electrólisis del agua.
Aunque parece que esta tecnología muy poco probable, ya que los ocho co-autores del trabajo científico - los chinos, no hay que olvidar que se está trabajando en el Departamento de Ciencia de los Materiales y Tecnología, la Universidad de Stanford, una de las instituciones científicas más prestigiosas del mundo
.
La reacción catalítica de las nanopartículas de óxido de metal (hierro, cobalto, óxidos de níquel o mezclas de sus óxidos) de aproximadamente 20 nm se convierte electroquímicamente en nanopartículas ultrapequeñas NiFeO x sub> con un diámetro de 2-5 nm como resultado de las reacciones inducidas por litio. A diferencia de la síntesis química tradicional, los autores de la invención, este método permite mantener una conexión eléctrica superior entre las nanopartículas y los resultados en la formación de gran superficie para la reacción catalítica.
Durante el experimento se probó el funcionamiento continuo del dispositivo de esta manera para una semana (200 horas) sin degradación de los electrodos, говорит Y Tsui (Yi Cui), uno de los autores del trabajo científico. Añadió que la eficiencia de la electrólisis del agua es de 82% a temperatura ambiente (al parecer, a presión normal, también).
Los resultados del estudio опубликованы 23 de junio 2015 en la revista Nature Communications (en libre acceso).
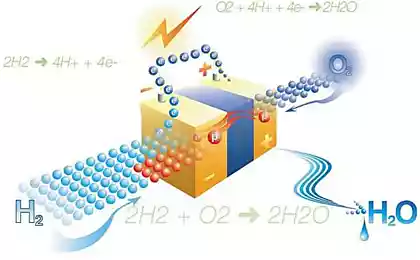
Como se ha señalado hace un año, este es un proyecto muy importante porque simplifica en gran medida la tecnología de fabricación de pilas de combustible e hidrógeno. En tales células puede operar electrónicos móviles y automóviles.

Toyota Mirai, una de primer coche del mundo en pilas de combustible de hidrógeno. Sales comenzaron 12.15.2014, bajo la parte inferior de sus dos cilindros con hidrógeno a una presión de 70 MPa. Reabastecimiento de combustible tarda 3-5 minutos. Rango de velocidad: 480 kilometros i>
Es importante que la combustión del hidrógeno único subproducto de la combustión es agua. La misma agua que se divide en componentes, como la luz solar en la primera etapa del proceso técnico.
Fuente: geektimes.ru/post/252516/
Los fans de Fallout recibirán el juego de Bethesda Fallout 4 por sus tapas de botellas
Tendencias de inversión: auge Robótica